Cho thêm 24,8 gam Na2O vào 375,2 gam dung dịch NaOH 10% thì thu được dung dịch mới có nồng độ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Na2O=0,5 mol
Na2O+H2O->2NaOH
0,5-----------------1 mol
ta có m NaOH=1.40+40=80g
=>C%=\(\dfrac{80}{431}100=18,561\%\)

Đáp án : C.
Xét Na : n H 2 = 1 2 n N a = a 46 m o l
Bảo toàn khối lượng :
mdd sau = mNa + m H 2 O – m H 2 = a + p – 2. a 46 (g)
=> C%NaOH = x %
Xét Na2O
=> mdd sau = m N a 2 O + m H 2 O = b + p
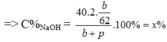
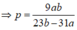

Bài 1 :
a)
$m_{NaOH} = 60.20\% = 12(gam)$
$m_{dd} = 60 + 40 = 100(gam)$
$C\%_{NaOH} = \dfrac{12}{100}.100\% = 12\%$
b)
$m_{dd} = 60 - 10 = 50(gam)$
$C\%_{NaOH} = \dfrac{12}{50}.100\% = 24\%$
Bài 2 :
a)
$m_{HNO_3} = 60.20\% = 12(gam)$
$m_{dd} = 60 + 200 = 260(gam)$
$C\%_{HNO_3} = \dfrac{12}{260}.100\% = 4,62\%$
b) Khi cô cạn 400 gam nước thì không còn nước trong dd trên nên không tồn tại dd

mNaOH=100.5%=5g
Gọi mddNaOH thêm =x(g)
=>mNaOH=0,2x
Tổng mNaOH=0,2x+5
Tổng mdd=x+100
=>0,2x+5=(x+100)0,1
=>0,1x=5=>x=50g

\(Na_2O+H_2O\rightarrow2NaOH\)
Khối lượng NaOH ban đầu:
\(m_{NaOH}=\dfrac{500.10}{100}=50g\)
Khối lượng NaOH được tạo ra từ Na2O:
\(m_{NaOH}=2.n_{Ca_2O}.M_{NaOH}=2.\dfrac{31}{62}.40=40g\)
Khối lượng NaOH sau cùng là: 50 + 40 = 90g
Khối lượng dd sau: 31 + 500 = 531g
Nồng độ % dd NaOH:
\(C\%_{NaOH}=\dfrac{90}{531}.100\%=16,95\%\)

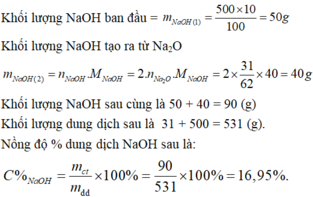
Bước 1: Tính khối lượng NaOH có trong dung dịch ban đầu
NaOH = 10% × 375,2g = 37,52 gam
Bước 2: Tính số mol Na₂O
Na₂O có M = 62 g/mol
→ n = 24,8 / 62 = 0,4 mol
Phản ứng:
Na₂O + H₂O → 2NaOH
Vậy 0,4 mol Na₂O tạo ra 0,8 mol NaOH
→ Khối lượng NaOH tạo thêm = 0,8 × 40 = 32 gam
Bước 3: Tính tổng khối lượng dung dịch sau phản ứng
Tổng khối lượng = 375,2g (ban đầu) + 24,8g (Na₂O) = 400 gam
Bước 4: Tính tổng khối lượng NaOH trong dung dịch mới
NaOH ban đầu: 37,52 gam
NaOH tạo thành: 32 gam
Tổng: 69,52 gam
Bước 5: Tính nồng độ phần trăm mới
C% = (69,52 / 400) × 100% = 17,38%
Vậy nồng độ mới của dung dịch NaOH là khoảng 17,4%.