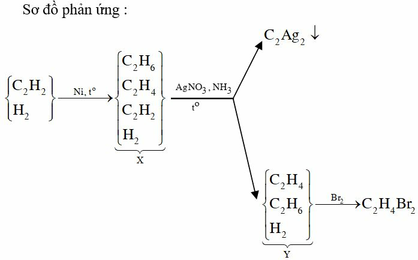
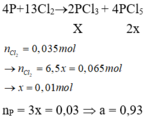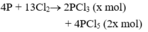Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni, đun nóng bình 1 thời gian, thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào lượng dư dung dịch AgNO3 trong NH3 đến phản ứng hoàn toàn, thu được hỗn hợp khí Y và 12 gam kết tủa. Hỗn hợp khí Y phản ứng vừa đủ với bao nhiêu mol Br2 trong dung dịch.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


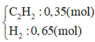
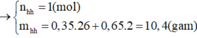
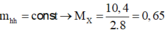
![]()
![]()
![]()
![]()

Đáp án A
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni.
Nung bình → hhX có dX/H2 = 8.
Theo BTKL: mhhX = mhh ban đầu = 0,35 x 26 + 0,65 x 2 = 10,4 gam
→ nhhX = 10,4 : 16 = 0,65 mol.
→ nH2phản ứng = nhh ban đầu - nX = 0,35 + 0,65 - 0,65 = 0,35 mol.
Ta có: nπ trước phản ứng = 2 x nCH≡CH = 2 x 0,35 = 0,7 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,7 - 0,35 = 0,35 mol.
• Ta có nπ dư = 2 x nAgC≡CAg + nBr2
→ nBr2 = 0,35 - 2 x (12 : 240) = 0,25 mol

Đáp án : B
C2H2
→
N
H
4
C
l
,
C
u
C
l
2
CH≡C-CH=CH2 + C2H2 dư
Gọi số mol C2H2 ban đầu là x,
Với H= 60% nên số mol C4H4 là
x
.
0
,
6
3
= 0,2x mol, số mol C2H4 dư là 0,4x
Khi tham gia phản ứng với AgNO3/NH3 sinh ra kết tủa chứa CAg≡C-CH=CH2: 0,3x mol; CAg≡ CAg : 0,4 x mol
→ 159. 0,3x + 0,4x . 240 = 43,11 → x = 0,3 mol
Vậy ∑ m = 0,3. 26 = 7,8 gam. Đáp án B

Đáp án C
Một bình kín chứa 0,04 mol C2H2; 0,06 mol H2, một ít Ni.
Nung → hhY.
hhY + Br2 dư thì có 0,04 mol hhZ thoát ra. dZ/H2 = 4,5.
• Theo bảo toàn khối lượng: mC2H2 + mH2 = mbình brom tăng + mZ
→ mbình brom tăng = 0,04 x 26 + 0,06 x 2 - 0,04 x 9 = 0,8 gam