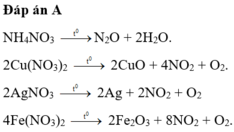Nhận biết các chất sau: KNO3, NH4NO3, Fe(NO3)2, AgNO3, HNO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Cho dung dịch NaOH lần lượt vào từng mẫu thử :
- Kết tủa xanh lam : Cu(OH)2
- Kết tủa trắng xanh sau đó hóa nâu đỏ trong không khí : Fe(NO3)2
- Kết tủa nâu đỏ : Fe(NO3)3
- Sủi bọt khí mùi khai : NH4NO3
- Kết tủa đen : AgNO3
- Kết tủa keo trắng , tan dần trong NaOH dư : Al(NO3)3
- Kết tủa trắng bền : Mg(NO3)2
- Không hiện tượng : NaNO3
PTHH em tự viết nhé !

Để xác định số oxy của các chất, ta cần phân tích công thức hóa học của từng chất.
K2S: Số oxy trong K2S là 0.HClO3: Số oxy trong HClO3 là 3.HClO4: Số oxy trong HClO4 là 4.K2Cr2O7: Số oxy trong K2Cr2O7 là 7.HNO3: Số oxy trong HNO3 là 3.FeO: Số oxy trong FeO là 1.Fe(NO3)3: Số oxy trong Fe(NO3)3 là 9.NH3: Số oxy trong NH3 là 0.H2S: Số oxy trong H2S là 0.H2SO4: Số oxy trong H2SO4 là 4.Fe(SO4): Số oxy trong Fe(SO4) là 4.NaNO3: Số oxy trong NaNO3 là 3.MgSO4: Số oxy trong MgSO4 là 4.FexOy: Không thể xác định số oxy của FexOy vì không biết cụ thể giá trị x và y.Cl2: Số oxy trong Cl2 là 0.N2O: Số oxy trong N2O là 1.SO2: Số oxy trong SO2 là 2.KNO3: Số oxy trong KNO3 là 3.CrCl3: Số oxy trong CrCl3 là 0.FeCl2: Số oxy trong FeCl2 là 0.AgNO3: Số oxy trong AgNO3 là 3.Vậy, số oxy của các chất là:
K2S: 0
HClO3: 3
HClO4: 4
K2Cr2O7: 7
HNO3: 3
FeO: 1
Fe(NO3)3: 9
NH3: 0
H2S: 0
H2SO4: 4
Fe(SO4): 4
NaNO3: 3
MgSO4: 4
FexOy: Không xác định
Cl2: 0
N2O: 1
SO2: 2
KNO3: 3
CrCl3: 0
FeCl2: 0
AgNO3: 3

Các dung dịch tạo được muối sắt II là: FeCl3, CuSO4, Pb(NO3)2, AgNO3 => Đap an B

Câu 2:
\(n_{AgNO_3}=\dfrac{25,5}{170}=0,15(mol)\\ PTHH:NaCl+AgNO_3\to AgCl\downarrow +NaNO_3\\ \Rightarrow m_{NaCl}=0,15.58,5=8,775(g)\)
Câu 3:
\(a,\)Đặt \(\begin{cases} n_{Mg}=x(mol)\\ n_{Zn}=y(mol) \end{cases} \Rightarrow 24x+65y=15,75(1)\)
\(PTHH:Mg+2HCl\to MgCl_2+H_2\\ Zn+2HCl\to ZnCl_2+H_2\\ \Rightarrow 95x+136y=44,15(2)\\ (1)(2)\Rightarrow \begin{cases} x=0,25(mol)\\ y=0,15(mol) \end{cases} \Rightarrow \begin{cases} \%_{Mg}=\dfrac{0,25.24}{15,75}.100\%=38,1\%\\ \%_{Zn}=100\%=38,1\%=61,9\% \end{cases} \)
\(b,\Sigma n_{HCl}=2n_{Mg}+2n_{Zn}=0,8(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{36,5.0,8}{10\%}=292(g)\)

NH4NO3 → t o N2O + 2H2O.
2Cu(NO3)2 → t o 2CuO + 4NO2 + O2.
2AgNO3 → t o 2Ag + 2NO2 + O2
4Fe(NO3)2 → t o 2Fe2O3 + 8NO2 + O2.
Đáp án A

Đáp án A.
NH4NO3 → N2O + 2H2O.
2Cu(NO3)2 → 2CuO + 4NO2 + O2.
2AgNO3 → 2Ag + 2NO2 + O2
4Fe(NO3)2 → 2Fe2O3 + 8NO2 + O2.

Đáp án A.
NH4NO3![]() N2O + 2H2O.
N2O + 2H2O.
2Cu(NO3)2![]() 2CuO + 4NO2 + O2.
2CuO + 4NO2 + O2.
2AgNO3![]() 2Ag + 2NO2 + O2
2Ag + 2NO2 + O2
4Fe(NO3)2![]() 2Fe2O3 + 8NO2 + O2.
2Fe2O3 + 8NO2 + O2.

Đáp án A.
NH4NO3 → t o N2O + 2H2O.
2Cu(NO3)2 → t o 2CuO + 4NO2 + O2.
2AgNO3 → t o 2Ag + 2NO2 + O2
4Fe(NO3)2 → t o 2Fe2O3 + 8NO2 + O2.