
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CaCO3+ H2SO4-> CaSO4+CO2+H2O
0.05 0.05
-> khối lượng bình A sau phản ứng tăng 5-0.05x44=2.8 g
cân trở lại vị trí cân bằng -> khối lượng bình B cũng tăng 2.8g
->4,787 - 44nC(X) = 2,8
-> nC(X) = nX = 1,987/44 (cái này không làm tròn thì PTK của X ra đúng hơn!)
->Mx= 106
-> A : Na2CO3

- Oxit bazo:
+, Li2O : Liti oxit
+, Na2O : Natri oxit
+, MgO: Magie oxit
+, Al2O3 : Nhôm oxit
- Oxit axit:
+, CO: cacbon monooxit
+, CO2 : cacbon đioxit
+, NO: nitơ monooxit
+, N2O5 : đinitơ pentaoxit
+, N2O3 : đinitơ trioxit

Ở Việt Nam có loại quặng hematit ( Fe 2 O 3 ) ở Trại Cau, tỉnh Thái Nguyên.. Vì vậy, nước ta đã xây dựng khu công nghiệp gang - thép ở Thái Nguyên...


PTHH: Zn + H2SO4 ===> ZnSO4 + H2\(\uparrow\)
a) Do Cu không tác dụng với H2SO4 (loãng) => 4,48 lít khí là sản phẩm của phản ứng giữa Zn và H2SO4
nH2 = 4,48 / 22,4 = 0,2 (mol)
=> nZn = nH2 = 0,2 (mol)
=> mZn = 0,2 x 65 = 13 (gam)
=> mCu = 20 - 13 = 7 (gam)
b) Thoe phương trình trên, nH2SO4 = nH2 = 0,2 mol
=> mH2SO4 = 0,2 x 98 = 19,6 (gam)
\(\Rightarrow C\%_{H2SO4}=\frac{19,6}{196}.100\%=10\%\)

a. PTHH: \(2SO_2+O_2\rightarrow^{t^o}_{V_2O_5}2SO_3\) (đoạn này Latex OLM đánh nhiều hơi rối nên không hiểu thì hỏi nhé)
\(SO_3+H_2O\rightarrow H_2SO_4\)
\(300ml=0,3l\)
\(\rightarrow n_{H_2SO_4}=1.0,3=0,3mol\)
Theo phương trình \(n_{O_2}=n_{SO_3}=n_{H_2SO_4}=0,3mol\)
\(\rightarrow m_{SO_2}=64.0,3=19,2g\)
b. PTHH: \(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
\(n_{Al_2O_3}=\frac{15,3}{102}=0,15mol\)
Xét tỉ lệ \(n_{Al_2O_3}>\frac{n_{H_2SO_4}}{3}\)
Vậy \(Al_2O_3\) dư
Theo phương trình \(n_{Al_2\left(SO_4\right)_3}=\frac{1}{3}n_{H_2SO_4}=0,1mol\)
\(\rightarrow C_{M_{Al_2\left(SO_4\right)_3}}=\frac{0,1}{0,3}=0,33M\)

15 tấn = 15 000(kg)
$m_{CaCO_3} = 15000.90\% = 13500(kg)$
$n_{CaCO_3} = \dfrac{13500}{100} = 135(kmol)$
$n_{CaCO_3\ pư} = 135.85\% = 114,75(kmol)$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
Theo PTHH : $n_{CaO} = n_{CaCO_3} = 114,75(kmol)$
$m_{CaO} = 114,75.56 = 6426(kg)$
Giải đáp thắc mắc :
100 là phân tử khối của $CaCO_3$
56 là phân tử khối của $CaO$
Cách làm như ảnh trên là áp số tỉ lệ về khối lượng theo PTHH

a. PTHH: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
b. Có \(n_{Mg}=\frac{3,6}{24}=0,15mol\)
\(140ml=0,14l\)
\(n_{H_2SO_4}=0,14.1,2=0,168mol\)
Lập tỉ lệ \(\frac{n_{Mg}}{1}< \frac{n_{H_2SO_4}}{1}\)
Vậy Mg đủ, \(H_2SO_4\) dư
Theo phương trình \(n_{H_2SO_4}=n_{Mg}=0,15mol\)
\(\rightarrow n_{H_2SO_4\left(\text{(dư)}\right)}=0,168-0,15=0,018mol\)
\(\rightarrow m_{H_2SO_4\left(\text{(dư)}\right)}n.M=0,018.98=1,764g\)
c. MgSO\(_4\) là muối
Theo phương trình \(n_{MgSO_4}=n_{Mg}=0,15mol\)
\(\rightarrow m_{\text{muối}}=m_{MgSO_4}=n.M=0,15.120=18g\)
d. \(H_2\) là khí
Theo phương trình \(n_{H_2}=n_{Mg}=0,15mol\)
\(\rightarrow V_{H_2\left(ĐKTC\right)}=n.22,4=0,15.22,4=3,36l\)
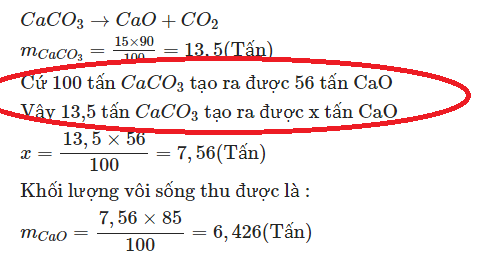
Rồng bay ở Thăng Long và đáp ở Hạ Long
đr bạn tick cái này cho mình đi mình tick cho bạn