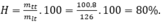Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(\text{a) N2+3H2->2NH3}\)
\(\text{4NH3+5O2->4NO+6H2O}\)
\(\text{2NO+O2->2NO2}\)
\(\text{O2+4NO2+2H2O->4HNO3}\)
b)
nN2=112000/22,4=5000(mol)
=>nHNO3=10000(mol)
hao hụt 15%
=>nHNO3=8500(mol)
\(\Rightarrow\text{mdd HNO3=8500x63/63%=850000(g)=0,85(tấn)}\)

\(\text{Ta có 2 N2 ----> 1 HNO3}\)
..............56.................63
................x.......................1000
\(\Rightarrow\text{x=(1000.56)/63=888,889 kg}\)
\(\Rightarrow\text{m N2 thực tế =888,889.100/75=1185,185 Kg}\)
\(\Rightarrow\text{V N2= 1185,185 .22,4/28=948,148 m^3 }\)
Để sản xuất 1 tấn HNO\(_3^{}\), người ta cần 0,5 tấn N\(_2^{}\), vì:
2N\(_2^{}\) + 6H\(_2^{}\) → 4NH\(_3^{}\)
4NH\(_3^{}\) + 5O\(_2^{}\) → 4NO + 6H\(_2^{}\)O
4NO + 2O\(_2^{}\) → 4NO\(_2^{}\)
4NO\(_2^{}\) + 2H\(_2^{}\)O + O\(_2^{}\) → 4HNO\(_3^{}\)
Mà: Chúng ta nhận thấy số mol N\(_2^{}\) bằng \(\frac12\) số mol HNO\(_3^{}\) nên:
1∙\(\frac12\)=0,5
Chọn A
Ta có khối lượng HNO 3 thực tế thu được là:
m tt = m HNO 3 = 160.63% = 100,8 tấn.
Sơ đồ điều chế HNO3 từ NH3
Lượng HNO 3 thu được theo lý thuyết là: m lt = x = (34.63):17=126 tấn.
Hiệu suất của phản ứng là