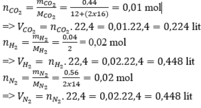Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

-\(m_{O_2}=n.M=0,2.32=6,4\left(g\right)\)
-\(m_{H_2}=n.M=0,5.2=1\left(g\right)\)
-\(n_{CO_2}=\dfrac{12.10^{23}}{6.10^{23}}=2\left(mol\right)\)
\(m_{CO_2}=n.M=2.44=88\left(g\right)\)
Thể tích ở đk nào

Câu 9:
1) nSO2 = 2,24 : 22,4 = 0,1 mol
nO2 = 3,36 : 22,4 = 0,15 mol
mhh = 0,1 . 64 + 0,15 . 32 = 11,2
2. nCO2 = 4,4 : 44 = 0,1 mol
nO2 = 3,2 : 32 = 0,1 mol
Vhh = (0,1 + 0,1 ) . 22,4 = 4,48 l
3. n = \(\frac{3.10^{23}}{6.10^{23}}=0,5mol\)
Câu 10 :
1. C2H5OH + 3O2 -> 2CO2 + 3H2O
2. Tỉ lệ : 1 : 3 : 2 : 3
3.

nSO2=m:M=6,4:64=0,1(mol)
VSO2=n.22,4=0,1.22,4=2,24(l)
nCO2=m:M=4,4:44=0,1(mol)
VCO2=n.22,4=0,1.22,4=2,24(l)
nH2=S:6.1023=1,2.1023:6.1023=0,2(mol)
VH2=n.22,4=0,2.22,4=4,48(l)
\(a.n_{SO_2}=\dfrac{m}{M}=\dfrac{6,4}{64}=0,1\left(mol\right)\\ n_{CO_2}=\dfrac{m}{M}=\dfrac{4,4}{44}=0,1\left(mol\right)\\ \Rightarrow n_{hh}=n_{SO_2}+n_{CO_2}=0,1+0,1=0,2\left(mol\right)\\ \Rightarrow V_{hh}=n.22,4=0,2.22,4=4,48\left(l\right)\)
\(n_{H_2}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2\left(mol\right)\Rightarrow V_{H_2}=n.22,4=0,2.22,4=4,48\left(l\right)\)

16 nCO2=0,2mol
PTHH: 2CO+O2=>2CO2
0,2<--0,1<---0,2
=> mO2=0,2.32=6,4g
=> khối lượng Oxi phản ứng với H2 là :
9,6-6,4=3,2g
=> nH2O=3,2:32=0,1mol
PTHH: 2H+O2=>H2O
b)
0,2<-0,1<-0,2
=> mH2=2.0,2=0,4g
mCO =0,2.28=5,6g
=> m hh=5,6+0,4=6g
CuO+H2-to--->Cu+H2O
0,6----0,6
nCuO =48/80=0,6 (mol)
==>VH2 =0,6×22,4=13.44(l)
17.
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\)
\(m_{H_2SO_4}=200.19,6\%=39,2g\)
\(n_{H_2SO_4}=\dfrac{39,2}{98}=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,1 < 0,4 ( mol )
0,1 0,1 0,1 0,1 ( mol )
\(V_{H_2}=0,1.22,4=2,24l\)
Chất còn dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,1\right).98=29,4g\)
\(\left\{{}\begin{matrix}m_{FeSO_4}=0,1.152=15,2g\\m_{H_2}=0,1.2=0,2g\end{matrix}\right.\)
\(m_{ddspứ}=5,6+200-0,1.2=205,4g\)
\(\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{15,2}{205,4}.100=7,4\%\\C\%_{H_2}=\dfrac{0,2}{205,4}.100=0,09\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{29,4}{205,4}.100=14,31\%\end{matrix}\right.\)