Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(a) Vì khi cho chất rắn thu được sau phản ứng với CO tác dụng với dung dịch HCl tạo ra khí H2 nên R phải là kim loại đứng sau Al và đứng trước hidro trong dãy hoạt động hóa học. Đặt công thức oxit của R là RxOy.
CuO + CO → Cu + CO2
a a
RxOy + yCO → xR + y CO2
c xc
Al2O3 + 6HCl → RCln + n/2 H2
xc nxc xc nxc/2
Đạt các mol CuO, Al2O3, RxOy trong 6,1 g hỗn hợp A là a,b,c. Có
80a + 102b+ (xMr + 16y)c = 6,1
1,28 + 102b + Mrxc = 4,82
64a = 1,28
6b + nxc = 0,15
nxc/2 = 0,045
=> a = 0,02
=> nxc = 0,09
b = -0,01
Mr = 28n
=> n = 2 , Mr = 56, R là Fe
xc = 0,45 => yc = 0,06
x/y = 0,045/0,06 = 3/4
=> x = 3, y = 4 CT oxit = Fe2O3
bạn ơi bài trên giải sai thì phải
sao al2o3+có lại được rcln+h2

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

1.
nO2 = 0,35 mol
Đặt nCO = x (mol); nH2 = y (mol); ( x, y > 0 )
2CO + O2 \(\underrightarrow{t^o}\) 2CO2 (1)
x......0,5x
2H2 + O2 \(\underrightarrow{t^o}\) 2H2O (2)
y.......0,5y
Từ (1)(2) ta có hệ pt
\(\left\{{}\begin{matrix}28x+2y=11,8\\0,5+0,5y=0,35\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}x=0,4\\y=0,3\end{matrix}\right.\)
\(\Rightarrow\) %mCO = \(\dfrac{0,4.28.100}{11,8}\approx94,9\%\)
\(\Rightarrow\) %mH2 = \(\dfrac{0,3.2.100}{11,8}\approx5,1\%\)
\(\Rightarrow\) %VCO = \(\dfrac{0,4.22,4.100}{\left(0,4.22,4\right)+\left(0,3.22,4\right)}\approx57,1\%\)
\(\Rightarrow\) %VH2 = \(\dfrac{0,3.22,4.100}{\left(0,4.22,4\right)+\left(0,3.22,4\right)}\approx42,9\%\)
3.
Đặt nCuO = x (mol); nAl2O3 = y (mol); ( x, y > 0 )
CuO + CO \(\underrightarrow{t^o}\) Cu + CO2
Ta có hệ pt
\(\left\{{}\begin{matrix}80x+102y=9,1\\64x+102y=8,3\end{matrix}\right.\)
\(\Rightarrow\) \(\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\Rightarrow\) mCuO = 0,05.80 = 4 (g)

Phương trình hóa học:
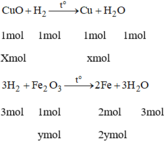
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
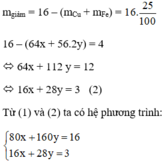
Giải hệ phương trình ta được: