Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol Cuo và Fe2O3 lần lượt là a,b
CuO + H2 = Cu + H2O
a a a (mol)
Fe2O3 + 3H2 = 2Fe +3H2O
b 3b 2b (mol)
Ta có hệ phương trình: 80a +160b= 40
64a + 112b= 29,6
=> a= 0,2 (mol) ; b= 0,15 (mol)
Số mol H2 phản ứng : 0,2 + 3 x 0,15= 0,65 (mol)
Số mol H2 đã dùng là: 0,65 : 75 x 100= 0,8 (mol)
Thể tích H2 là 0,8 x 22,4= 17,92 (L)
Khối lượng cu trong hỗn hợp là: 0,2 X 64 = 12,8 (g)
%mCu= 12,8 : 29,6 X 100= 43,2%
%mFe= 100%- 43,2%= 56,8%
có mấy cái gần bằng nha bạn, mình không chắc đúng k thử tham khảo nha

Ta có:
\(n_{H2}=\frac{0,448}{22,4}=0,02\left(mol\right)\)
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(CuO+H_2\rightarrow Cu+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow n_{Fe}=n_{H2}=0,02\left(mol\right)\)
\(\Rightarrow n_{Fe2O3}=\frac{1}{2}n_{Fe}=0,01\left(mol\right)\)
\(\Rightarrow m_{Fe2O3}=0,01.160=1,6\left(g\right)\)
\(\left\{{}\begin{matrix}\%_{Fe2O3}=\frac{1,6}{24}.100\%=6,67\%\\\%m_{CuO}=100\%-6,67\%=93,33\%\end{matrix}\right.\)
\(n_{Cu}=n_{CuO}=0,28\left(mol\right)\)
\(\Rightarrow m=m_{Fe}+m_{Cu}=0,02.56+0,28.64=19,04\left(g\right)\)

Bai 1
Ta co pthh
2Al + 6HCl \(\rightarrow\)2AlCl3 + 3H2
Mg + 2HCl \(\rightarrow\)MgCl2 + H2
a,Theo de bai ta co
Khoi luong cua moi chat trong 1 mol hon hop la
mAl=\(\dfrac{36.7,5}{100}=2,7g\)
mMg = 7,5 - 2,7 =4,8 g
So mol cua moi chat la
nAl=\(\dfrac{2,7}{27}=0,1mol\)
nMg=\(\dfrac{4,8}{24}=0,2mol\)
b,Theo 2 pthh ta co
nH2=\(\dfrac{3}{2}nAl=\dfrac{3}{2}.0,1=0,15mol\)
nH2=nMg=0,2 mol
\(\Rightarrow\)VH2=(0,15 + 0,2 ) .22,4=7,84 l
Bai 2 ta co pthh
CuO + H2 \(\rightarrow\)Cu + H2O
Fe2O3 + 3H2\(\rightarrow\)2Fe + 3H2O
Theo de bai ta co
nH2 =\(\dfrac{25,76}{22,4}=1,15mol\)
Goi x mol la so mol cua H2 tham gia vao pthh1
So mol cua H2 tham gia vao pthh 2 la 1,15-x mol
Theo pthh
nCuO =nH2=x mol
nFe2O3=\(\dfrac{1}{3}nH2=\dfrac{1}{3}.\left(1,15-x\right)mol\)
Theo de bai ta co he pt
80x + 160.\(\dfrac{1}{3}\left(1,15-x\right)\)=68
\(\Leftrightarrow\)80x + 61,3 -53,3x =68
\(\Leftrightarrow\)26,7x =6,7
\(\Rightarrow\)x=0,3 mol
\(\Rightarrow\)nFe2O3 =\(\dfrac{1}{3}nH2=\dfrac{1}{3}.0,3=0,1mol\)
nCuO=nH2 =0,3 mol
\(\Rightarrow\)thanh phan % khoi luong la
%mCuO =\(\dfrac{\left(0,3.80\right).100}{68}\approx35,3\%\)
%mFe2O3= 100 -35,3=64,7 %

mhh giảm=16/100.25=4(g)
mhh giảm =mH2O
pt:
CuO+H2--->Cu+H2O
x______________x
Fe2O3+3H2--->2Fe+3H2O
y__________________3y
Hệ pt:
\(\left\{{}\begin{matrix}80x+160y=16\\18x+54y=4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=\dfrac{7}{45}\\y=\dfrac{1}{45}\end{matrix}\right.\)
=>mCuO
=>%mCuO
=>%mFe2O3

Giải:
Số mol H2 là:
nH2 = V/22,4 = 6,72/22,4 = 0,3 (mol)
PTHH: CuO + H2 -> Cu + H2O
----------x------x-------x------x--
PTHH: Fe2O3 + 3H2 -> 2Fe + 3H2O
------------y--------3y-----2y-----3y--
Gọi nCuO = x (mol) và nFe2O3 = y (mol)
Ta có hpt:
\(\left\{{}\begin{matrix}mCuO+mFe2O3=20\left(g\right)\\nH2=0,3\left(mol\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}80x+160y=20\left(g\right)\\x+3y=0,3\left(mol\right)\end{matrix}\right.\)
Giải hpt, được:
\(\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
Phần trăm khối lượng mỗi kim loại:
%mCuO = (mct/mhh).100 = (0,15.80/20).100 = 60 %
=> %mFe2O3 = 100 - 60 = 40 %
Vậy ...
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Gọi a,b lần lượt là sm của CuO, Fe2O3 trong hh (a,b>0)
Ta có: \(\left\{{}\begin{matrix}80a+160b=20\\a+3b=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,15\\b=0,05\end{matrix}\right.\)
\(\Rightarrow\%m_{CuO}=\dfrac{0,15.80}{20}.100\%=60\%\)
\(\Rightarrow\%m_{Fe_2O_3}=40\%\%0\).
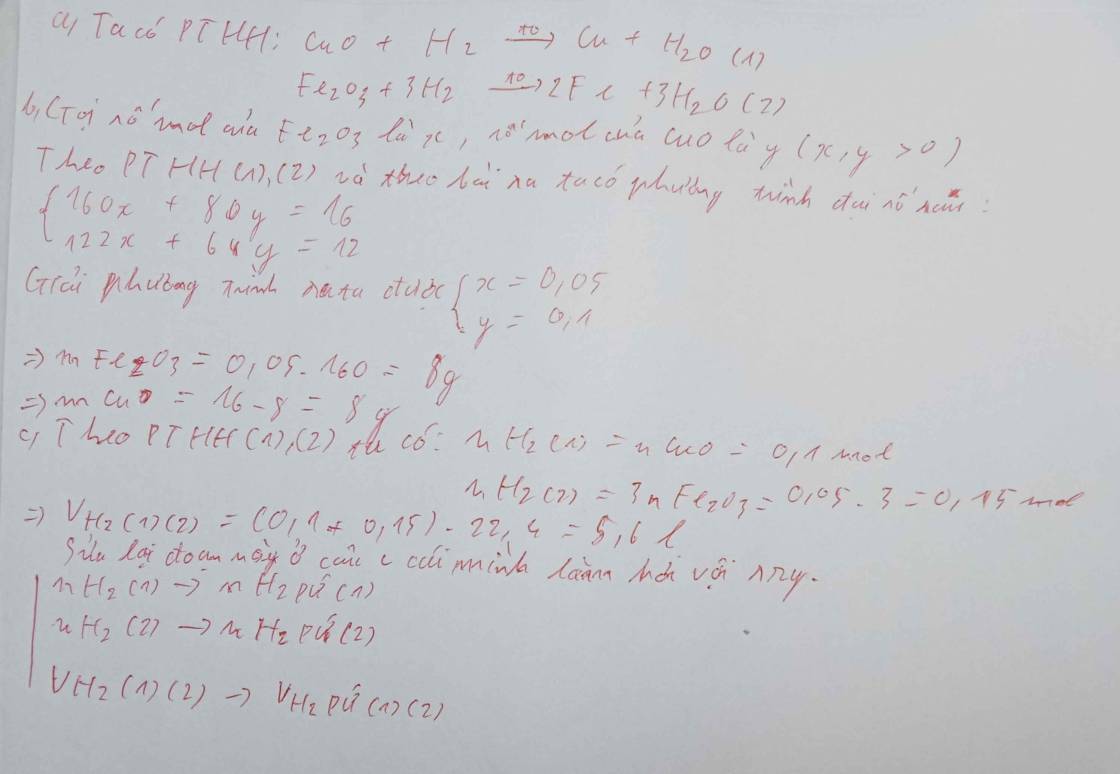
CuO+H2--->Cu+H2O
x______x____x
Fe2O3+3H2--->2Fe+3H2O
y_______3y____2y
Hệ pt:
\(\left\{{}\begin{matrix}80x+160y=16\\64x+112y=12\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,05\end{matrix}\right.\)
mCu=0,1.64=6,4(g)
mFe=0,05.2.56=5,6(g)
mCuO=0,1.80=8(g)
=>%mCuO=8/16.100%=50%
=>%mFe2O3=100%-50%=50%