Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

khi nung hỗn hợp Al và Fe2O3, CuO thì đã có phản ứng nhiệt nhôm.
2Al + Fe2O3 ---> Al2O3 + 2Fe
2a<--- a --------------------> 2a
2Al + 3CuO ---> Al2O3 + 3Cu
2b<--- 3b -----------------> 3b
theo giả thiết: 160a + 240b = 37,6 (1)
ta có n_NO = 0,4 mol => n_electron thu = 1,2 mol => n_electron nhường = 1,2 mol
=> 6a + 6b = 1,2(2)
từ (1) và (2) => a = 0,13, b = 0,07
=> tổng số mol Al là 2a + 2b = 0,4 mol => m_Al = 10,8 (g)

Giải thích:
Na : x mol ; Al : y mol và Al2O3 : z mol
→ 23x + 27y + 102z = 9,8
Na + H2O → NaOH + ½ H2
2NaOH + 2Al + H2O→ NaAlO2 + 3H2
2NaOH + Al2O3 → 2NaAlO2 + H2O
→ dung dịch Y có NaAlO2 : y + 2z mol, NaOH : x – y - 2z
Y + HCl
NaAlO2 + HCl + H2O → NaCl + Al(OH)3
∆nHCl = 0,195 mol
Kết tủa có m2 < m1
→ TH2 tạo kết tủa hoàn toàn rồi tan một phần
→ nHCl(1) = x – y – 2z + n↓(1)
nHCl(2) = x – y – 2z + y + 2z + 3. ( y + 2z – n↓(2))
→ n↓(2) – n↓(1) = - 0,025
= ![]() → x = 0,16
→ x = 0,16
→%Na= 37,55%
Đáp án B

Giải thích:
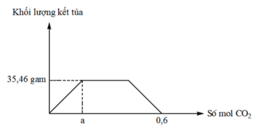
nBaCO3max = 35,46/ 197 = 0,18 (mol)
nBa2+ = nBaCO3 max = 0,18 (mol) tại thời điểm nCO2 = a (mol)
=> nCO2 = a = 0,18 (mol)
Khi mol CO2 = 0,6 (mol) thì kết tủa tan hết, dung dịch thu được chứa Ba2+ (0,18 mol), HCO3- ( 0,6 mol) , Na+ (x mol)
Bảo toàn điện tích => nNa+ = 0,6.1 – 0,18.2 = 0,24 (mol)
Bảo toàn electron: 2nBa + nNa = 2nH2 + 2nO
=> nO = ( 2. 0,18 + 0,24 – 2.0,18)/2 = 0,12 (mol)
=> m = mNa + mBa + mO = 0,24.23 + 0,18.137 + 0,12.16 = 32,1 (g)
Đáp án A

Đáp án B
Bảo toàn electron:
ne kim loại nhường = 4nO2 + 2nH2 = 4. 0,08 + 2.0,14 = 0,6 (mol)
=> dd Z chứa nOH- = 0,6 (mol)
Dd Z tác dụng với NaHCO3 dư => nBa2+ = nBaCO3 = 0,2 (mol)
Dd Z tác dụng với 0,45 mol CO2 => thu được nCO32- = 0,15 ; nHCO3- = 0,3 (mol)
=> mBaCO3 ↓ = 0,15.197 = 29,55 (g) ( Tính theo số mol của CO32-)

Giải thích:
Bảo toàn electron:
ne kim loại nhường = 4nO2 + 2nH2 = 4. 0,08 + 2.0,14 = 0,6 (mol)
=> dd Z chứa nOH- = 0,6 (mol)
Dd Z tác dụng với NaHCO3 dư => nBa2+ = nBaCO3 = 0,2 (mol)
Dd Z tác dụng với 0,45 mol CO2 => thu được nCO32- = 0,15 ; nHCO3- = 0,3 (mol)
=> mBaCO3 ↓ = 0,15.197 = 29,55 (g) ( Tính theo số mol của CO32-)
Đáp án B
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{15,6}{78}=0,2\left(mol\right)\), \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
BTNT Al, có: nAl = nAl(OH)3 = 0,2 (mol)
BT e,có: nNa + 3nAl = 2nH2 ⇒ nNa = 0,2 (mol)
\(\Rightarrow m=m_{Na}+m_{Al}=10\left(g\right)\)
Ta có: nAl(OH)3=15,678=0,2(mol)���(��)3=15,678=0,2(���), nH2=8,9622,4=0,4(mol)��2=8,9622,4=0,4(���)
BTNT Al, có: nAl = nAl(OH)3 = 0,2 (mol)
BT e,có: nNa + 3nAl = 2nH2 ⇒ nNa = 0,2 (mol)
⇒m=mNa+mAl=10(g)