Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

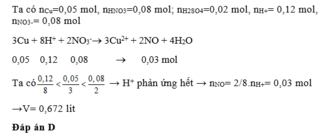
Ta có: nFe=0,02 mol; nCu= 0,03 mol, nH2SO4= 0,2 mol, nNaNO3= 0,08 mol
nH+= 2n H 2 S O 4 = 0,4 mol, n N O 3 -= 0,08 mol
3Cu + 8H+ + 2NO3-® 3Cu2+ + 2NO + 4H2O (1)
0,03 0,08 0,02 ® 0,03 mol
Fe + 4H+ + NO3- ® Fe3+ + NO + 2H2O (2)
0,02 0,08 0,02 ® 0,02 mol
Tổng số mol H+ tham gia phản ứng (1) và (2) là 0,08+ 0,08= 0,16 mol
→nH+ dư= 0,4-0,16= 0,24 mol
Dung dịch X có chứa Cu2+, Fe3+ và H+
H++ OH-→H2O (3)
Cu2++ 2OH- → Cu(OH)2 (4)
Fe3++ 3OH- → Fe(OH)3 (5)
Theo PT (3), (4), (5) ta có
nOH-= nH++ 2nCu2++ 3nFe3+= 0,24+ 2.0,03+ 3.0,02= 0,36 mol= nNaOH
→V= 0,36 lít= 360 ml
Đáp án A

nH+=0,4+0,1.a
nNO3-=0,1a
bạn viết phương trình Mg+H+ +NO3- dưới dạng pt ion
H++NO3 ttuowng đương với HNO3 loãng
rồi bạn sử dụng phương pháp đường chéo, định luật bảo toàn nguyên tố và electron

1) Toàn bộ quá trình có thể tóm tắt: Fe - 2e = Fe2+; N+5 + 3e = N+2; Cu - 2e = Cu2+;
Bảo toàn e: 2x + 2.2,08/64 = 3.(1,12+0,448)/22,4. Suy ra: x = 0,0725 mol. Vậy m = 56.0,0725 = 4,06g.
2) Gọi x là số mol Fe, suy ra Cu có số mol là 2x.
Ta có: 64.2x + 56x = 2,76 suy ra: x = 0,015 mol.
Cu - 2e = Cu2+; Fe - 3e = Fe3+; N+5 + 3e = NO + NO2
Bảo toàn e: số mol (NO+NO2) = 1/3(2.0,03 + 3.0,015) = 0,035 mol.
V = 22,4.0,035 = 0,784 lít.

Ta thấy trong X có các ancol có đặc điểm: số C = số nhóm OH
=> Khi đốt cháy X : \(n_{CO_2}=n_{C\left(X\right)}=n_{OH}=0,25mol\)
=> Khi phản ứng vớ Na => \(n_{H_2}=\frac{1}{2}n_{OH}=0,125mol\)
=> V = 2,8 lít

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam
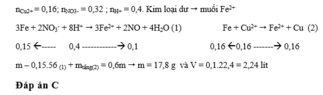
Chọn C
Do sau phản ứng thu được hỗn hợp kim loại nên có các phản ứng: