Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B.
Lời giải
Ta có thể tích khí giảm chính là thể tích H2 phản ứng
⇒ V H 2 p h ả n ứ n g = V + 3V - 2V = 2V (lít) => H2 dư
Vì phản ứng xảy ra hoàn toàn, H2 dư ⇒ V H 2 p h ả n ứ n g = 2Vandehit
=> anđehit no, 2 chức hoặc anđehit đơn chức và có một liên kết đôi (1)
Lại có: anđehit + H2 ancol
=> Trong Y gồm V lít ancol và V lít H2 dư => Z là ancol
Có n H 2 sin h r a t ừ p h ả n ứ n g c ộ n g N a = nancol => ancol có 2 chức (2)
Từ (1) và (2) suy ra anđehit no, hai chức, mạch hở

N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do hiệu suất phản ứng là 25% nên
VN2 pứ= 4.25%= 1 lít; VH2 pứ= 12.25%= 3 lít;
VNH3 sinh ra= 2VN2 pứ= 2 lít
VN2 dư= 4-1=3 lít, VH2 dư= 12-3=9 lít
Hỗn hợp thu được sau phản ứng có thể tích là
V= VN2 dư+ VH2 dư+ VNH3 sinh ra= 3 +9+2=14 lít
Đáp án B

Đáp án B.
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 25 1 > 60 3 →Hiệu suất tính theo H2
Đặt thể tích H2 phản ứng là x lít
→VN2 pứ= x/3 lít, VNH3 sinh ra=2x/3 lít
VN2 dư= 25-x/3 (lít), VH2 dư= 60- x(lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 60-x+ 25-x/3+ 2x/3= 75
→ x=15 lít

Đáp án : C
Ta có Cùng điều kiện -> Quy số lít về số mol.n(hh ban đầu) = 20 mol; n(hh sau) = 16 lít
=> H2 phản ứng mất 4 lít => C2H2 có 2 lít và CH4 có 8 lít

Chọn đáp án C
Ta có phản ứng
1N2 + 3H2 ⇌ 2NH3
Hiệu suất tính theo N2 vì:  .
.
nN2 pứ = ![]()
⇒ Hpứ =![]()

Đáp án A.
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do 4 1 < 14 3 →Hiệu suất tính theo N2
Đặt thể tích N2 phản ứng là x lít
→VH2 pứ= 3x lít, VNH3 sinh ra=2xlít
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được là
V khí= VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4
→ x=0,8 lít
→ H = v N 2 pu V N 2 bd · 100 % = 0 , 8 4 · 100 % = 20 %

Đáp án C
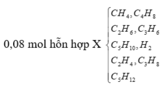
![]()
Vì phản ứng xảy ra hoàn toàn mà nanken < 0,08 nên hỗn hợp Y chứa ankan và H2 dư
→ nanken = 0,2 + 0,08- 0,25 = 0,03 mol
→ nankan (CH4, C2H6+ C3H8+ C5H12 dư) + H2 = 0,08- 0,03= 0,05
→ ∑ nC5H12 ban đầu = 0,05 mol
Đốt cháy hoàn toàn Y tương đương đốt cháy 0,05 mol C5H12 và 0,2 mol H2
→ nCO2 = 0,25 mol, nH2O = 0,05.6 + 0,2 = 0,5 mol
→ mdd = 0,25. 44 + 0,5.18-0,25. 100 = -5 gam .
Vậy dung dịch giảm 5 gam
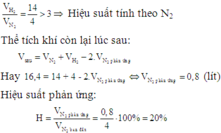
Ta có: \(n_{N_2}=0,2\left(mol\right)\)
\(n_{H_2}=0,3\left(mol\right)\)
PT: \(N_2+3H_2⇌2NH_3\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,3}{1}\)
Vậy: Nếu pư hoàn toàn thì H2 hết.
⇒ Tính theo số mol H2.
Mà: H% = 25%
\(\Rightarrow n_{H_2\left(pư\right)}=0,3.25\%=0,075\left(mol\right)\)
Theo PT: \(n_{NH_3}=\dfrac{2}{3}n_{H_2}=0,05\left(mol\right)\)
\(\Rightarrow V_{NH_3}=0,05.22,4=1,12\left(l\right)\)
Bạn tham khảo nhé!