Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khi lên cao thêm 10m thì áp suất khí quyển giảm 1mmHg vậy lên 3140m giảm 3140/10=314 mmHg
Từ PV/T= const ta có:
P1V1/T1=P2V2/T2
mà V=m/D.thay vào ta được:
P1m/T1D1 = P2m/T2D2 =>D2=P2T1D1/P1T2
thay số vào:
D2 = (446x273x1,29)/(760x275) =0,75Kg/m^3

Bài giải:
+ Trạng thái 1:
p1 = (760 – 314) mmHg
T1 = 273 + 2 = 275 K
V1 = mp1mp1
Trạng thái 2:
p0 = 760 mmHg
T0 = 273 K
\(V=\dfrac{m}{p_0}\)
Phương trình trạng thái:
\(\dfrac{poVo}{T_0}=\dfrac{p_1V_1}{T_1}\Rightarrow\dfrac{p_0.m}{p_0T_0}=\dfrac{p_1.m}{p_1.T_1}\)
\(\Rightarrow p_1=\dfrac{p_1p_0T_0}{p_0T_1}=\dfrac{446.1,29.273}{760.275}\)
p1 = 0,75 kg/m3

Gọi \(m_1;m_2\) là khối lượng khí trong bình trước và sau khi đun nóng bình. Áp dụng phương trình Menđêlêep - Clapêrông ta có: \(pV=\frac{m_1}{\mu}RT_1;pV=\frac{m_2}{\mu}RT_2\)
Từ đó suy ra khối lượng khí đã thoát ra:
\(m_2-m_1=\frac{pV\mu}{R}\left(\frac{1}{T_1}-\frac{1}{T_2}\right)\), với \(p=50atm,V=10\)lít \(,\mu=2g\)
\(R=0,084atm.l\text{/}mol.K;\)\(T_1=7+273=280K\)
\(T_2=17+273=290K\). Suy ra \(m_2-m_1=1,47g\)
Gọi m1,m2m1,m2 là khối lượng khí trong bình trước và sau khi đun nóng bình. Áp dụng phương trình Menđêlêep - Clapêrông ta có: pV=m1μRT1,pV=m2μRT2pV=m1μRT1,pV=m2μRT2
Từ đó suy ra khối lượng khí đã thoát ra:
m2−m1=pVμR(1T1−1T2)m2−m1=pVμR(1T1−1T2), với p=50atm,V=10lít,μ=2gp=50atm,V=10lít,μ=2g
R=0,084atm.l/mol.K;T1=7+273=280KR=0,084atm.l/mol.K;T1=7+273=280K
T2=17+273=290KT2=17+273=290K. Suy ra m2−m1=1,47g

Bài giải.
+ Trạng thái 1:
p1 = 750 mmHg
T1 = 300 K
V1 = 40 cm3
+ Trạng thái 2 :
P0 = 760 mmHg
T0 = 273 K
V0 = ?
+ Phương trình trạng thái :
\(\dfrac{p_0V_0}{T_0}=\dfrac{p_1V_1}{T_1}\Rightarrow V_0=\dfrac{p_1V_1}{T_1}.\dfrac{T_0}{p_0}\)
\(V_0=\dfrac{750.40.273}{760.300}=36cm^3\)

Áp dụng pt trạng thái: (P1.V1):T1= (P2.V2):T2
<=> (750x40):300= (760.V2):273
Giải pt tìm được V2

Trạng thái 1 { V 1 = 4 ( l ) T 1 = 7 + 273 = 280 K
Trạng thái 2 { V 2 = m ρ 2 T 2 = ?
Áp dụng định luật Gay – Luyxắc
V 1 V 2 = T 1 T 2 ⇒ T 2 = T 1 . V 2 V 1 ⇒ T 2 = T 1 V 1 . m ρ 2 = ( 273 + 7 ) .12 4.1 , 2 T 2 = 700 0 K ⇒ t 2 = T 2 − 273 = 327 0 C
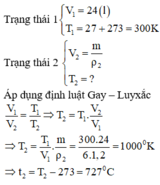

Câu 1.
Trạng thái 1: \(\left\{{}\begin{matrix}p_1\\T_1\end{matrix}\right.\)
Trạng thái 2: \(\left\{{}\begin{matrix}p_2=p_1+\dfrac{1}{40}p_1\\T_2=T_1+20\end{matrix}\right.\)
Quá trình đẳng tích:
\(\dfrac{p_1}{T_1}=\dfrac{p_2}{T_2}\Rightarrow\dfrac{p_1}{T_1}=\dfrac{p_1+\dfrac{1}{40}p_1}{T_1+20}\Rightarrow T_1=800K=527^oC\)
Câu 2.
Ở đktc có \(p_0=1atm\Rightarrow m=\rho_0\cdot V_0\)
Ở \(0^oC\) có \(p=150atm\Rightarrow m=\rho\cdot V\)
Khối lượng vật không đổi.\(\Rightarrow\rho_0\cdot V_0=\rho\cdot V\)
\(\Rightarrow\rho=\dfrac{\rho_0\cdot V_0}{V}=\dfrac{1,43\cdot150}{1}=214,5\)kg/m3
\(V=10l=10dm^3=0,01m^3\)
Khối lượng khí \(O_2\) thu được tại thời điểm \(0^oC\) là:
\(m=\rho\cdot V=214,5\cdot0,01=2,145kg\)