Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1,
V1, N1 là thể tích, nồng độ of HCl
V2, N2 là thể tích, nồng độ of Na2CO3
Sử dụng công thức V1 N1 = V2 N2
==> N2 = 0.42 (N)
--> C = 0.21 (M)
--> m =0.6678 g. Vậy hàm lượng Na2CO3 là 0.6678g trong 2g ngậm nc.
2,
Pha dung dịch 0.1M: cần 10.6g Na2CO3 tinh khiết. Trong 2g muối thì có 0.6678g Na2CO3 --> cần dùng 35.3934g muối trên --> định mức 1L (1000ml)

Khi đốt mẫu gang trong oxi, cacbon cháy tạo thành C O 2 . Dẫn C O 2 qua nước vôi trong dư, toàn bộ lượng C O 2 chuyển thành kết tủa C a C O 3 .
C + O 2 → t ° C O 2 (1)
C O 2 + C a ( O H ) 2 → C a C O 3 ↑ + H 2 O (2)
Theo các phản ứng (1) và (2): n c = n C O 2 = n C a C O 3 = 0,01 (mol)
Khối lượng cacbon: m C = 0,01.12 = 0,12 (g)
Hàm lượng (%) cacbon trong mẫu gang:
%C = 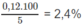

1) \(n_{HCl\left(bđ\right)}=10^{-3}.0,02=0,00002\left(mol\right)\)
\(\Rightarrow C_{MddHCl}=\dfrac{0,00002}{0,02}=0,001\left(M\right)\)
\(\Rightarrow\left[H^+\right]=C_{MddHCl}=0,001M\)
\(pH=-log\left(0,001\right)=3\)
Chúc bạn học tốt
2) \(n_{HCl}=10^{-4}.0,03=0,000003\left(mol\right)\)
\(\Rightarrow C_{MddHCl}=\dfrac{0,000003}{0,03}=0,0001\left(M\right)\)
\(\Rightarrow\left[H^+\right]=C_{MddHCl}=0,0001M\)
\(pH=-log\left(0,0001\right)=4\)
Chúc bạn học tốt

1) mNaOH nguyên chất=50*25%=12,5g
2)m dd=\(\dfrac{mđường}{c\%}\)
=50/25%=200g
c%dd nc đường=\(\dfrac{50}{50+mnước}=\dfrac{25}{100}\)
-> m nước=150g
3)n Zn=0,1 mol
nHCl=0,4 mol
hcl dư tính theo Zn
BTE: 2*nZn=2*nH2
=>nH2=nZn=0,1 mol
=>V=2,24l
tổng m chất tan=m hcl dư+mZnCl2=(0,4-0,2)*36,5+0,1*136=20,9g
c%HCl dư=\(\dfrac{0,2\cdot36,5}{6,5+100-0,1\cdot2}\cdot100\%=6,87\%\)
c%ZnCl2=\(\dfrac{0,1\cdot136}{6,5+100-0,2}\cdot100\%=12,8\%\)

Nếu bạn còn cần
Mà thôi, tui viết kiến thức cho, gặp mấy bài kiểu này còn biết làm chứ
\(\dfrac{n_{OH^-}}{n_{H_3PO_4}}=T\)
\(\left[{}\begin{matrix}H_3PO_4+NaOH\rightarrow NaH_2PO_4+H_2O\left(1\right)\\H_3PO_4+2NaOH\rightarrow Na_2HPO_4+2H_2O\left(1\right)\\H_3PO_4+3NaOH\rightarrow Na_3PO_4+3H_2O\left(3\right)\end{matrix}\right.\)
\(T< 1\Rightarrow chi-xay-ra-\left(1\right)\Rightarrow H_3PO_4\left(du\right);H_2PO_4^-\)
\(T=1\Rightarrow H_2PO_4^-\)
\(1< T< 2\Rightarrow xay-ra-\left(1\right)-va-\left(2\right)\Rightarrow H_2PO_4^-;HPO_4^{2-}\)
\(T=2\Rightarrow HPO_4^{2-}\)
\(2< T< 3\Rightarrow xay-ra-\left(2\right)va\left(3\right)\Rightarrow HPO_4^{2-};PO_4^{3-}\)
\(T=3\Rightarrow PO_4^{3-}\)
\(T>3\Rightarrow chi-xay-ra-\left(3\right)\Rightarrow PO_4^{3-};OH^-\left(du\right)\)
Còn đâu bạn chỉ việc viết phương trình và làm như bài hóa lớp 8 :v