Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Theo định luật Faraday ta có khối lượng chất thoát ra ở điện cực là :
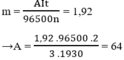
Trong đó A là nguyên tử khối
A = 64 ⇒ A là Cu

\(a.Catot:M^{2+}+2e\rightarrow M\\ Anot:2H_2O\rightarrow4H^++O_2+4e\\ PTHH:2MSO_4+2H_2O-^{đp}\rightarrow2M+O_2+2H_2SO_4\\ b.m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,92\\ \Rightarrow A=64\left(Cu\right)\)

Đáp án A
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+chưa điện phân hết
Tại t (s):
Catot: Cu2+ + 2e → Cu
0,16 ←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu Anot: 2Cl- → Cl2 + 2e
0,36 ←0,18 2x x 2x
2H2O + 2e → 2OH- + H2. 2H2O → 4H+ + O2 + 4e
2y→4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)

Đáp án A
Do khi ta điện phân tiếp mà khối lượng catot vẫn tiếp tục tăng chứng tỏ ở t (s) thì Cu2+chưa điện phân hết
Tại t (s):
Catot: Cu2++2e→Cu
0,16←0,08
Tiếp tục điện phân tiếp 2t (s) nghĩa là tại 3t (s):
Catot:
Cu2+ + 2e → Cu
Anot: 2Cl- → Cl2 + 2e
0,36←0,18
2H2O + 2e → 2OH- + H2.
2x x 2x
2H2O → 4H+ +O2 + 4e
2y → 4y → y→ 4y
Tại t = 3t (s) thì số mol e trao đổi gấp 3 lần tại t(s)
→ n(e trong quá trình tạo H2) = 0,16. 3 – 0,36 = 0,12 → n(H2) = 0,06
BT e: 2x + 4y = 0,48
Tổng số mol khí: x + y + 0,06 = 0,28
→ x = 0,2 và y = 0,02 → m = 0,18. 160 + 0,4. 74,5 = 58,6 (g)
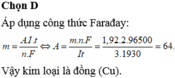

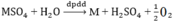


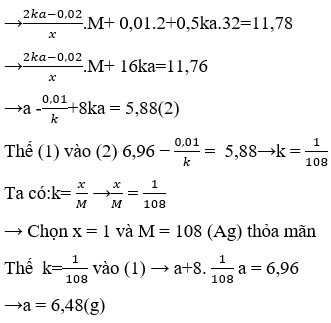
\(m=\dfrac{AIt}{nF}=\dfrac{A.3.1930}{2.96500}=1,95=>A=65\left(Zn\right)\)