Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

đặt \(m_{quặng}\)= a(g).
Ta có: \(m_{CaCO_3}\)= 0,8.a (g)
=> n\(_{CaCO_3}\)=\(\dfrac{0,8.a}{100}\)=0,008.a (mol)
Vì H%=90% => n\(_{CaO}\)\(_{Thu}\)\(_{được}\)=0,008.a.0,9=0,0072.a(mol)
Ta có : n\(_{CaO}\)\(_{Thu}\)\(_{được}\)= \(\dfrac{7000000}{56}\)=125000(mol).
=> 0,0072.a=125000 => a=17361111,11(g)
=17,36111 ( tấn)
Vậy cần 17,36111 tấn quặng
đặt ���ặ��mquặng= a(g).
Ta có: �����3mCaCO3= 0,8.a (g)
=> n����3CaCO3=0,8.�1001000,8.a=0,008.a (mol)
Vì H%=90% => n���CaO�ℎ�Thuđượ�được=0,008.a.0,9=0,0072.a(mol)
Ta có : n���CaO�ℎ�Thuđượ�được= 700000056567000000=125000(mol).
=> 0,0072.a=125000 => a=17361111,11(g)
=17,36111 ( tấn)
Vậy cần 17,36111 tấn quặng

Bài toán:
Hỗn hợp \(A\) gồm \(N_{2}\) và \(H_{2}\). Tỉ khối hơi của \(A\) đối với \(H_{2}\) là 15. Sau khi nung có xúc tác thích hợp, thu được hỗn hợp \(B\) với tỉ khối hơi đối với \(H_{2}\) là 8,5.
Câu hỏi:
a) Tính phần trăm thể tích \(N_{2}\) trong hỗn hợp trước và sau phản ứng.
b) Tính hiệu suất phản ứng.
Giải quyết:
Phần a) Tính phần trăm thể tích của \(N_{2}\) trong hỗn hợp trước và sau phản ứng
1. Tính tỉ khối hơi của hỗn hợp \(A\) đối với \(H_{2}\):
- Tỉ khối hơi của hỗn hợp \(A\) đối với \(H_{2}\) được cho là 15. Tỉ khối hơi (so với \(H_{2}\)) có thể tính bằng công thức:
\(\text{T}ỉ\&\text{nbsp};\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{h}o\text{i} = \frac{\text{Kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{mol}\&\text{nbsp};\text{trung}\&\text{nbsp};\text{b} \overset{ˋ}{\imath} \text{nh}\&\text{nbsp};\text{c}ủ\text{a}\&\text{nbsp};\text{h} \overset{\sim}{\hat{\text{o}}} \text{n}\&\text{nbsp};\text{h}ợ\text{p}}{\text{Kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{l}ượ\text{ng}\&\text{nbsp};\text{mol}\&\text{nbsp};\text{c}ủ\text{a}\&\text{nbsp}; H_{2}} .\)
- Khối lượng mol của \(H_{2}\) là \(M_{H_{2}} = 2\) g/mol.
- Giả sử hỗn hợp \(A\) có \(V_{1}\) thể tích của \(N_{2}\) và \(V_{2}\) thể tích của \(H_{2}\), ta có:
\(\text{T}ỉ\&\text{nbsp};\text{kh} \overset{ˊ}{\hat{\text{o}}} \text{i}\&\text{nbsp};\text{c}ủ\text{a}\&\text{nbsp};\text{A} = \frac{V_{1} M_{N_{2}} + V_{2} M_{H_{2}}}{V_{1} M_{H_{2}}} .\)
Với \(M_{N_{2}} = 28\) g/mol và \(M_{H_{2}} = 2\) g/mol, ta có:
\(\frac{V_{1} \cdot 28 + V_{2} \cdot 2}{V_{2} \cdot 2} = 15.\)
Giải phương trình này:
\(\frac{V_{1} \cdot 28 + V_{2} \cdot 2}{V_{2} \cdot 2} = 15 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } 28 \cdot \frac{V_{1}}{V_{2}} + 1 = 15.\)\(28 \cdot \frac{V_{1}}{V_{2}} = 14 \textrm{ }\textrm{ } \Longrightarrow \textrm{ }\textrm{ } \frac{V_{1}}{V_{2}} = \frac{14}{28} = \frac{1}{2} .\)
Vậy tỉ lệ thể tích giữa \(N_{2}\) và \(H_{2}\) trong hỗn hợp \(A\) là \(\frac{V_{1}}{V_{2}} = \frac{1}{2}\).
2. Tính phần trăm thể tích của \(N_{2}\) trong hỗn hợp \(A\):
- Gọi \(V_{2} = V\) là thể tích của \(H_{2}\), thì thể tích của \(N_{2}\) là \(V_{1} = \frac{V}{2}\).
- Tổng thể tích của hỗn hợp \(A\) là \(V_{1} + V_{2} = \frac{V}{2} + V = \frac{3 V}{2}\).
Vậy phần trăm thể tích của \(N_{2}\) trong hỗn hợp \(A\) là:
\(\text{Ph} \overset{ˋ}{\hat{\text{a}}} \text{n}\&\text{nbsp};\text{tr} \overset{ }{\text{a}} \text{m}\&\text{nbsp};\text{th}ể\&\text{nbsp};\text{t} \overset{ˊ}{\imath} \text{ch}\&\text{nbsp};\text{c}ủ\text{a}\&\text{nbsp}; N_{2} = \frac{V_{1}}{V_{1} + V_{2}} \times 100 \% = \frac{\frac{V}{2}}{\frac{3 V}{2}} \times 100 \% = \frac{1}{3} \times 100 \% = 33 , 33 \% .\)
Phần b) Tính hiệu suất phản ứng
1. Phản ứng xảy ra khi nung hỗn hợp \(A\):
Hỗn hợp \(A\) phản ứng theo phản ứng tổng hợp \(N H_{3}\) như sau:
\(N_{2} + 3 H_{2} \rightarrow 2 N H_{3} .\)
2. Tính tỉ khối hơi của hỗn hợp \(B\) đối với \(H_{2}\):
Tỉ khối hơi của hỗn hợp \(B\) đối với \(H_{2}\) là 8,5. Giả sử sau phản ứng, \(B\) gồm \(N_{2}\), \(H_{2}\), và \(N H_{3}\). Khi phản ứng xảy ra, \(N_{2}\) và \(H_{2}\) được sử dụng để tạo ra \(N H_{3}\). Chúng ta cần tính thể tích các chất trong hỗn hợp \(B\).
- Khối lượng mol của \(N H_{3}\) là \(M_{N H_{3}} = 17\) g/mol.
- Tỉ khối hơi của hỗn hợp \(B\) là 8,5, nghĩa là:
\(\frac{V_{1} M_{N_{2}} + V_{2} M_{H_{2}} + V_{N H_{3}} M_{N H_{3}}}{V_{1} M_{H_{2}}} = 8 , 5.\)
Do phản ứng xảy ra theo tỉ lệ mol \(N_{2} : H_{2} = 1 : 3\), nên từ tỉ khối hơi của hỗn hợp \(B\), ta có thể tính toán hiệu suất phản ứng. Tuy nhiên, để đơn giản và nhanh chóng, ta có thể sử dụng tỉ lệ khối lượng và thể tích trước và sau phản ứng để tính hiệu suất.
3. Tính hiệu suất phản ứng:
Hiệu suất phản ứng có thể tính bằng công thức:
\(\text{Hi}ệ\text{u}\&\text{nbsp};\text{su} \overset{ˊ}{\hat{\text{a}}} \text{t} = \frac{\text{S}ả\text{n}\&\text{nbsp};\text{ph}ẩ\text{m}\&\text{nbsp};\text{th}ự\text{c}\&\text{nbsp};\text{t} \overset{ˊ}{\hat{\text{e}}}}{\text{S}ả\text{n}\&\text{nbsp};\text{ph}ẩ\text{m}\&\text{nbsp};\text{l} \overset{ˊ}{\text{y}} \&\text{nbsp};\text{thuy} \overset{ˊ}{\hat{\text{e}}} \text{t}} \times 100 \% .\)
- Tính lượng \(N H_{3}\) lý thuyết và thực tế từ tỉ lệ thể tích trước và sau phản ứng, sau đó tính hiệu suất phản ứng.
Kết luận:
a) Phần trăm thể tích của \(N_{2}\) trong hỗn hợp trước phản ứng là 33,33%.
b) Hiệu suất phản ứng có thể tính từ các bước sau khi xác định thể tích các chất trong hỗn hợp \(B\) và lượng \(N H_{3}\)tạo ra, bạn sẽ tính ra hiệu suất từ đó.

a) Dần xuất hiện kết tủa trắng.
\(CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgNO_3\)
\(b)n_{CaCl_2}=\dfrac{2,22}{111}=0,02mol\\ n_{AgNO_3}=\dfrac{1,7}{170}=0,01mol\\ \Rightarrow\dfrac{0,02}{1}< \dfrac{0,01}{2}\Rightarrow CaCl_2.dư\\ CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\)
0,005 0,01 0,005 0,01
\(m_{AgCl}=0,01.143,5=1,435g\\ c)C_{M_{Ca\left(NO_3\right)_2}}=\dfrac{0,005}{0,07}=\dfrac{1}{14}M\\ C_{M_{CaCl_2.dư}}=\dfrac{0,02-0,005}{0,07}=\dfrac{3}{14}M\)

1. Đồng hydroxit
2 . Nitrous Oxide
3 . Barium Sulfate
4. Hydro Sulfide

P=> 1→1 P2O5 2→2 + H3PO4
H3PO4 3→
=> Na3PO4 4→
+ Ca3(PO4)2
(1) 4P + 5O2 ��→to 2P2O5
(2) P2O5 + 3H2O → 2H3PO4
(3) H3PO4 + NaOH → Na3PO4 + H2O
(4) 2Na3PO4 + 3CaCl2 → 6NaCl + Ca3(PO4)2

V hỗn hợp khí = V oxygen + V nitrogen = 1 x 24,79 + 4 x 24,79 = 123,95 lít

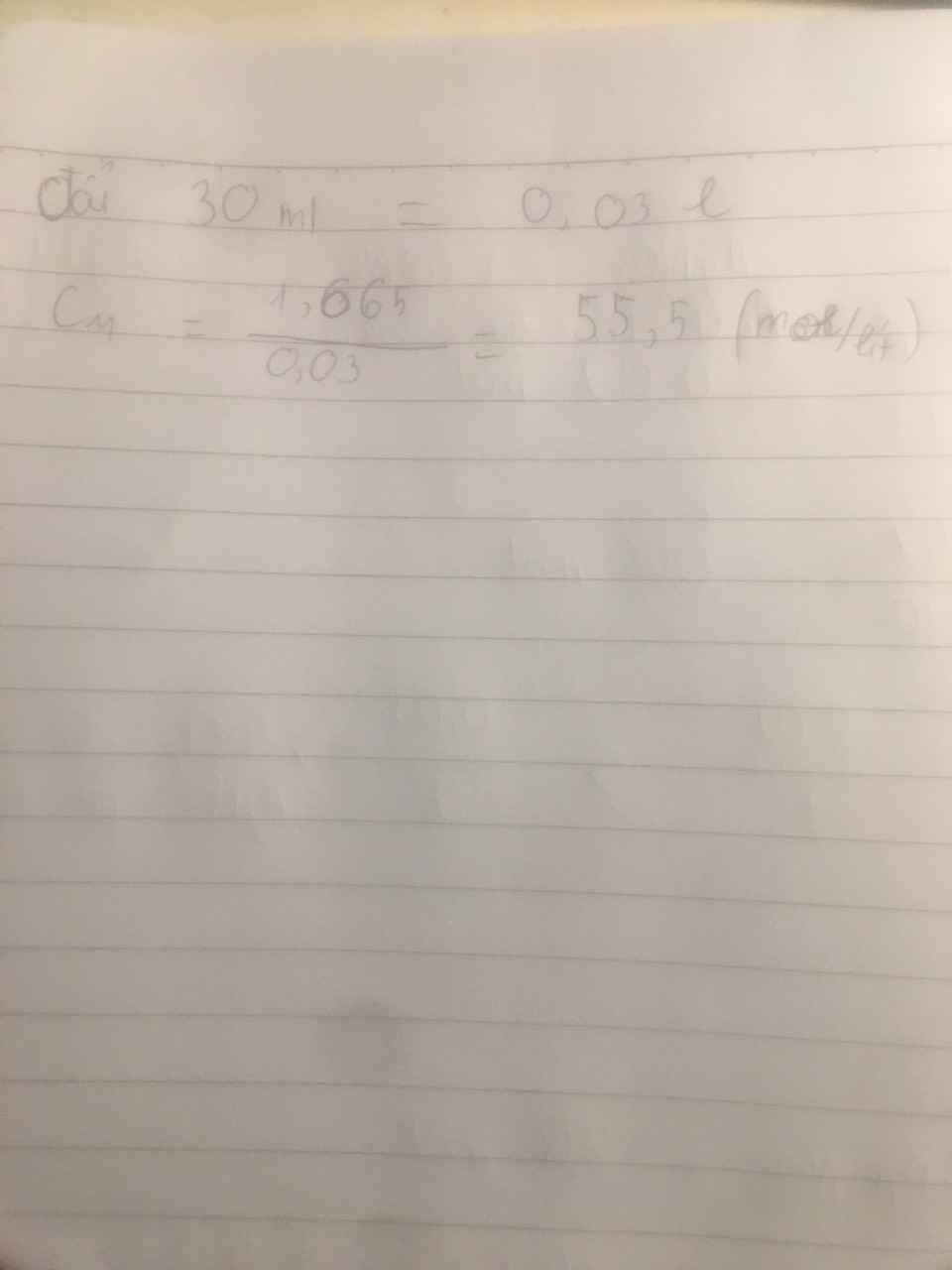
nO2=a;nN2=4a��2=�;��2=4�
PTHH: 2SO2+O2V2O5⟷2SO32��2+�2⟷�2�52��3
Bđ: a� a�
Pư: 2x2� x� 2x2�
Sau: a−2x�−2� a−x�−� 2x2�
Bảo toàn khối lượng: mA=mB⇒nA.