Hòa tan hoàn toàn 8,96 gam iron (Fe) trong dung dịch hydrochloric acid (HCl). Sau phản ứng thu được V lít khí hydrogen ở điều kiện chuẩn. Xác định giá trị của V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a)
Fe + S --to--> FeS
Fe + 2HCl --> FeCl2 + H2
FeS + 2HCl --> FeCl2 + H2S
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\); \(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,15}{1}\) => Fe hết, S dư
=> Chất sau khi nung gồm FeS, S dư
b)
PTHH: Fe + S --to--> FeS
0,1->0,1------->0,1
FeS + 2HCl --> FeCl2 + H2S
0,1-------------------->0,1
=> Y là H2S
VH2S = 0,1.22,4 = 2,24 (l)
c) Z là S
mS = (0,15 - 0,1).32 = 1,6 (g)

\(n_{khí}=n_{SO_2}=0,2\left(mol\right)\\ n_{hhkhí}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH:
2H2S + 3O2 --to--> 2H2O + 2SO2
0,2 <-------------------------------- 0,2
\(\rightarrow n_{H_2}=0,4-0,2=0,2\left(mol\right)\)
PTHH:
Fe + 2HCl ---> FeCl2 + H2
0,2 <------------------------ 0,2
FeS + 2HCl ---> FeCl2 + H2S
0,2 <-------------------------- 0,2
Fe + S --to--> FeS
0,2 <- 0,2 <---- 0,2
\(\rightarrow\left\{{}\begin{matrix}m_{Fe}=\left(0,2+0,2\right).56=22,4\left(g\right)\\m_S=0,2.32=6,4\left(g\right)\end{matrix}\right.\)
PTHH: SO2 + 2H2O + Br2 ---> H2SO4 + 2HBr
0,2 --------------> 0,2
\(\rightarrow m_{Br_2}=0,2.160=32\left(g\right)\)

cÂU 2.
\(n_Z=\dfrac{6,72}{22,4}=0,3mol\)
\(\left\{{}\begin{matrix}n_{CaCO_3}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\Rightarrow100x+56y=25,6\left(1\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(\Rightarrow x+y=n_Z=0,3\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\%m_{CaCO_3}=\dfrac{0,2\cdot100}{25,6}\cdot100\%=78,125\%\)
\(\%m_{Fe}=100\%-78,125\%=21,875\%\)
\(m_{muối}=m_{CaCl_2}+m_{FeCl_2}=0,2\cdot111+0,1\cdot127=34,9g\)

\(a,Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=\dfrac{V_{H_2\left(đkc\right)}}{24,79}=\dfrac{24,79}{24,79}=1\left(mol\right)\\ b,n_{Fe}=n_{H_2}=1\left(mol\right)\\ \Rightarrow m_{Fe}=M_{Fe}.n_{Fe}=56.1=56\left(g\right)\)
\(n_{H_2}=\dfrac{24,79}{22,4}=1,11mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(1,11\) \(\leftarrow\) 1,11
\(a=m_{Fe}=1,11\cdot56=62,16g\)

\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.2...................0.2..........0.2\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{FeCl_2}=0.2\cdot127=25.4\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=11.2+200-0.2\cdot2=210.8\left(g\right)\)
\(C\%_{FeCl_2}=\dfrac{25.4}{210.8}\cdot100\%=12.05\%\)
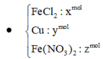
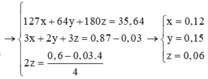
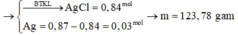

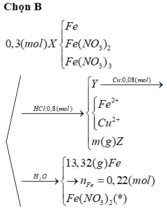

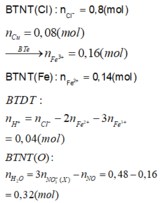
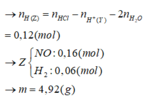
\(Fe+2HCl→\:FeCl_2+H_2\)
0,16 0,32 0,16 0,16
số mol Fe là:
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{8,96}{56}=0,16\left(mol\right)\)
thể tích khí H2 thoát ra là:
\(V_{H_2}=24,79\cdot n_{H_2}=24,79\cdot0,16=3,9664\left(L\right)\)