khi cho 2,4 g kim loại mg(II) phản ứng vừa đủ với dung dịch sulfuric acid h2SO4 loãng thu được muối iron sulfate MgSO4 và giải phòng khí hydrogen hcl = 0,6 n.
a) viết phương trình hóa học của phản ứng.
b) tính khối lượng muối MgSO4 thu được sau phản ứng.
c) tính thể tích khí h2 thu được sau phản ứng ở điều kiện chuẩn.


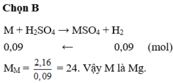
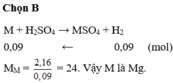
a, \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
b, \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo PT: \(n_{MgSO_4}=n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
\(\Rightarrow m_{MgSO_4}=0,1.120=12\left(g\right)\)
c, \(V_{H_2}=0,1.24,79=2,479\left(l\right)\)
a) Mg+H2SO4→MgSO4+H2Mg+H2SO4→MgSO4+H2
nMg=2,424=0,1(mol)nMg=2,424=0,1(mol)
nH2=nMg=0,1(mol)nH2=nMg=0,1(mol)
VH2=0,1.22,4=2,24(l)VH2=0,1.22,4=2,24(l)
b) nH2SO4=nMg=0,1(mol)nH2SO4=nMg=0,1(mol)
mddH2SO4=0,1.98.10010=98(g)mddH2SO4=0,1.98.10010=98(g)
c) nMgSO4=nMg=0,1(mol)nMgSO4=nMg=0,1(mol)
mMgSO4=0,1.120=12(g)mMgSO4=0,1.120=12(g)
mdd=2,4+98−0,1.2=100,2(g)