Câu 1: Zinc Zn tác dụng với sulfuric acid H2SO4 theo sơ đồ sau: Zn + H2SO4 → ZnSO4 + H2 Có 13 g Zinc tham gia phản ứng. Tính: a) Khối lượng acid tham gia phản ứng. b) Khối lượng muối zinc sulfate ZnSO4 tạo thành. c) Thể tích khí hydrogen thu được sau phản ứng (đkc).
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(m_{ct}=\dfrac{20.14,7}{100}=2,94\left(g\right)\)
\(n_{H2SO4}=\dfrac{2,94}{98}=0,03\left(mol\right)\)
Pt : \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2|\)
1 1 1 1
0,03 0,03 0,03
\(n_{Zn}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
⇒ \(m_{Zn}=0,03.65=1,95\left(g\right)\)
\(n_{H2}=\dfrac{0,03.1}{1}=0,03\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,03.22,4=0,672\left(l\right)\)
⇒ Chọn câu : D
Chúc bạn học tốt

Bài 1:
\(a)Mg+2HCl\rightarrow MgCl_2+H_2\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ b)Zn+2HCl\rightarrow ZnCl_2+H_2\\ Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
Bài 2:
\(a)Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ b)n_{H_2}=\dfrac{3,36}{22,4}=0,15mol\\ n_{Fe}=n_{H_2SO_4}=n_{H_2}=0,15mol\\ m_{Fe}=0,15.56=8,4g\\ c)C_{M_{H_2SO_4}}=\dfrac{0,15}{0,05}=3M\)

\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ 0,2........0,3...........0,1...........0,3\left(mol\right)\\ a.C_{MddH_2SO_4}=\dfrac{0,3}{0,3}=1\left(M\right)\\ b.m_{Al_2\left(SO_4\right)_3}=342.0,1=34,2\left(g\right)\\ c.V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)
PTHH: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{3}{2}n_{Al}=0,3\left(mol\right)\)
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,3}=1M\)
b) \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=n.M=0,1.342=34,2\left(g\right)\)
c) \(n_{H_2}=n_{H_2SO_4}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=n.22,4=0,3.22,4=6,72\left(l\right)\)

\(n_{Zn}=\dfrac{9,75}{65}=0,15\left(mol\right)\\
pthh:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,15 0,15 0,15 0,15
\(V_{H_2}=0,15.22,4=3,36L\\
m_{H_2SO_4}=0,15.98=14,7\left(g\right)\\
m_{ZnSO_4}=161.0,15=24,15g\\
\)
\(n_{CuO}=\dfrac{6}{80}=0,075\left(mol\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\
LTL:0,075< 0,15\)
=> H2 dư
\(n_{Cu}=n_{CuO}=0,075\left(mol\right)\\
m_{Cu}=0,075.64=4,8g\)
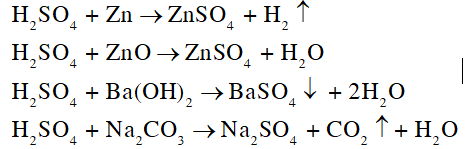
số mol của Zn là: n = m/M = 13/65 = 0,2 (mol)
a. khối lượng acid tham gia PỨ là: m = nM = 0,2 x 98 = 19,6 (g)
b. khối lượng muối ZnSO4 tạo thành là: m = nM = 0,2 x 161 = 32,2 (g)
c. thể tích khí H2 sau PỨ là: V = 24,79n = 24,79 x 0,2 = 4,958 (L)