Cho 2,4 gam Mg vào dung duịch chứa 0,02 mol Ag+ và 0,15 mol Cu2+. Khối lượng chất rắn thu được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Thứ tự các phản ứng xảy ra:
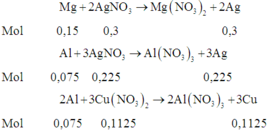
Vậy mchất rắn sau phản ứng = mAg + mCu = 108.0,525 + 64.0,1125 = 63,9 (gam)

n Mg = 0,25 mol.
Phản ứng : Mg + 2FeCl3 → 2FeCl2 + MgCl2
Mg + CuCl2 → MgCl2 + Cu
Mg + FeCl2 → Fe + MgCl2
=> Sau phản ứng tạo 0,12 mol Cu và 0,02 mol Fe
=> m A = 8,8g
=>D

Đáp án A
Theo ĐLBT ĐT thì 0,2.1+ 2x+ 0,3=0,7 suy ra x=0,1 mol
AgNO3→ Ag+ NO2+ ½ O2
Cu(NO3)2 →CuO+ 2NO2+ ½ O2
KNO3 →KNO2+ ½ O2
Chất rắn Y chứa Ag: 0,2 mol; CuO: 0,1 mol; KNO2: 0,3 mol
m=0,2.108+ 0,1.80+ 0,3.85=55,1 gam

Giải thích: Đáp án C
Hỗn hợp thu được gồm 2 kim loại là Cu và Ag
Bảo toàn e: ne( Cu2+; Ag+ nhận) > n e (Mg, Zn nhường)
=> 2.2 + 2.1 > 1,3.2 + x.2
=> x < 1,7 mol

Đáp án C
Hai kim loại thu được sau phản
ứng là Ag, Cu => Mg và Zn đều hết.
Áp dụng bảo toàn electron =>
![]()
![]()
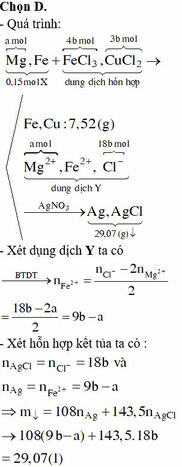

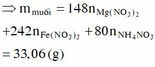


Ta có: nMg = 0,1 (mol)
\(Mg+2Ag^+\rightarrow Mg^{2+}+2Ag\)
0,01____0,02___________0,02 (mol)
\(Mg+Cu^{2+}\rightarrow Mg^{2+}+Cu\)
0,09____0,09___________0,09 (mol)
⇒ m chất rắn = mAg + mCu = 0,02.108 + 0,09.64 = 7,92 (g)