Đốt cháy 6,89g P trong KK thu đc 14,2g P2O5.Tính H%(TÍNH H THEO P)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a. 4P + 5O2 2P2O5
b. nP2O5 = \(\dfrac{2,84}{142}\)= 0,02 mol . Theo tỉ lệ phản ứng => nP = 2nP2O5 = 0,04 mol.
=>mP đã đốt cháy = 0,04.31 = 1,24 gam.
c. nO2 = 2,5nP2O5 = 0,05 mol
=> V O2 = 0,05.22,4 = 1,12 lít.
Mà oxi chiếm \(\dfrac{1}{5}\) thể tích không khí=> V không khí = VO2 . 5 = 5,6 lít.


- Số mol Al là: nAl=m.M=13,5.27=0,5(mol)
PTHH:4Al+3O2→2Al2O3
(mol) 4 3 2
(mol) 0,5 0,375 0,25
Thể tích của khí Oxi cần dùng là:
VO2=n.22,4=0,375.22,4=8,4(l)
\(n_{Al}=\dfrac{13,5}{27}=0,5\left(mol\right)\\ n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ Vì:\dfrac{0,5}{4}>\dfrac{0,2}{2}\Rightarrow Aldư\\ \Rightarrow n_{O_2}=\dfrac{3}{2}.n_{Al_2O_3}=\dfrac{3.0,2}{2}=0,3\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\)

PTHH : \(4Al+3O_2\left(t^o\right)->2Al_2O_3\) (1)
\(n_{Al_2O_3}=\dfrac{m}{M}=\dfrac{20,4}{27.2+16.3}=0,2\left(mol\right)\)
Từ (1) -> \(n_{O_2}=\dfrac{3}{2}n_{Al_2O_3}=0,3\left(mol\right)\)
-> \(V_{O_2\left(đktc\right)}=n.22,4=0,3.22,4=6,72\left(l\right)\)

a) nO2= 0,1(mol)
4P + 5 O2 -to-> 2 P2O5
b) nP= 4/5 . nO2=0,08(mol)
=>mP=0,08.31=2,48(g)
c) nP2O5=2/5. nO2= 0,04(mol)
=>mP2O5= 0,04.142=5,68(g)

Sửa câu b: tính kl oxi đã dùng
\(a,4P+5O_2\xrightarrow{t^o}2P_2O_5\\ b,\text{Bảo toàn KL: }m_P+m_{O_2}=m_{P_2O_5}\\ \Rightarrow m_{O_2}=7,1-3,1=4(g)\)
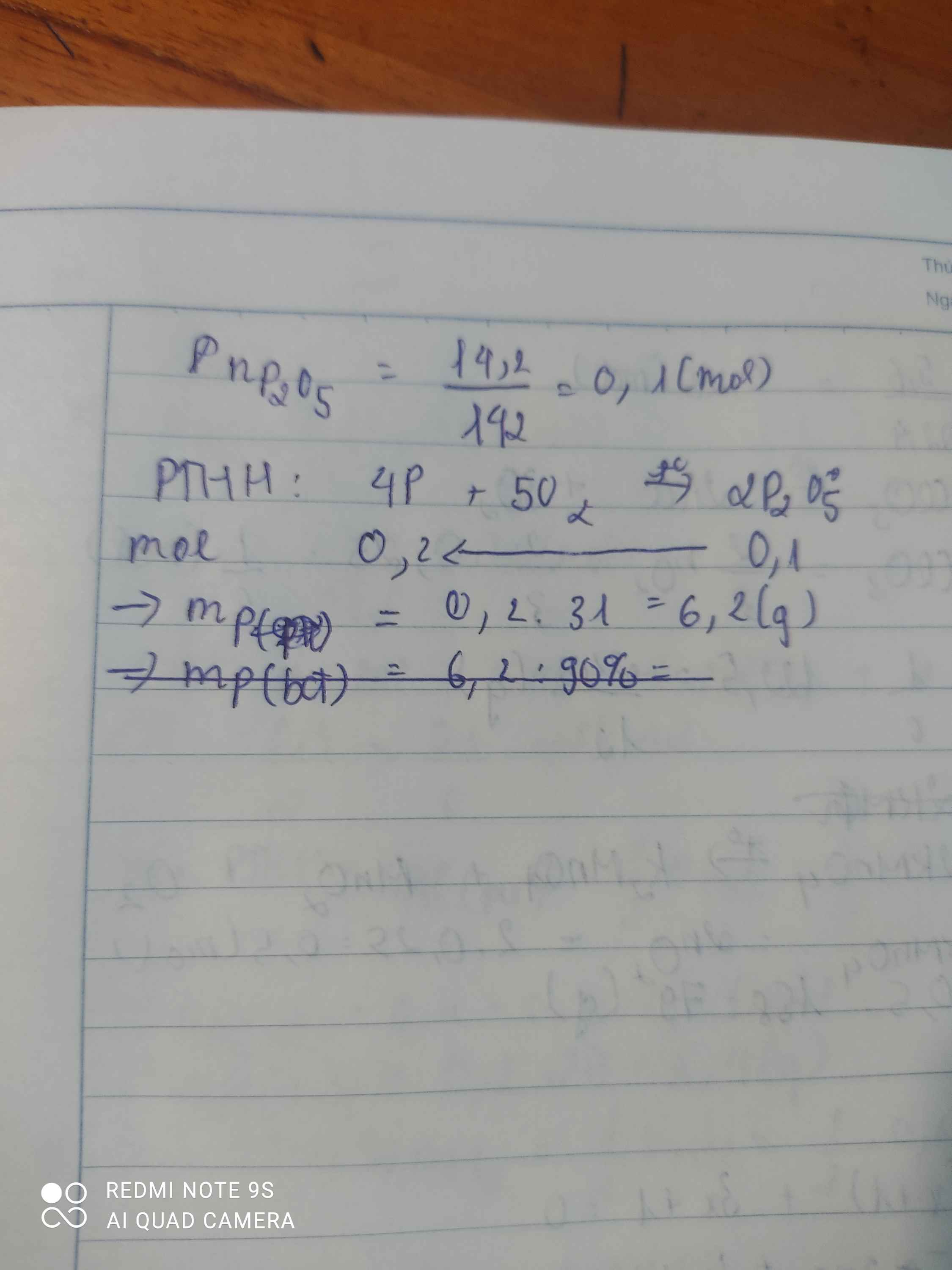
Ta có: \(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
PT: \(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
___0,2_________0,1 (mol)
\(\Rightarrow m_{P\left(pư\right)}=0,2.31=6,2\left(g\right)\)
Mà: mP (ban đầu) = 6,89 (g)
\(\Rightarrow H\%=\dfrac{6,2}{6,89}.100\%\approx89,99\%\)
Bạn tham khảo nhé!
4P+5O2-to>2P2O5
0,2---------------0,1 mol
n P2O5=\(\dfrac{14,2}{142}\)= 0,1 mol
m P pứ= 0,2.31=6,2g
=>H %=\(\dfrac{6,2}{6,89}\)=89,98%