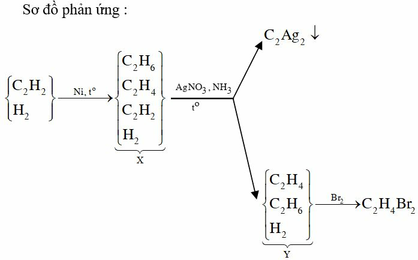
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni. Nung nóng bình một thời gian thu được hỗn hợp khí X có tỉ khối so với H2 bằng 8. Sục X vào dung dịch AgNO3 dư trong NH3 đến phản ứng hoàn toàn thu được hỗn hợp khí Y và 12 gam kết tủa. Hỗn hợp khí Y phản ứng vừa đủ với bao nhiêu mol Br2 trong dung dịch ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án : B
C2H2
→
N
H
4
C
l
,
C
u
C
l
2
CH≡C-CH=CH2 + C2H2 dư
Gọi số mol C2H2 ban đầu là x,
Với H= 60% nên số mol C4H4 là
x
.
0
,
6
3
= 0,2x mol, số mol C2H4 dư là 0,4x
Khi tham gia phản ứng với AgNO3/NH3 sinh ra kết tủa chứa CAg≡C-CH=CH2: 0,3x mol; CAg≡ CAg : 0,4 x mol
→ 159. 0,3x + 0,4x . 240 = 43,11 → x = 0,3 mol
Vậy ∑ m = 0,3. 26 = 7,8 gam. Đáp án B

Đáp án C
Một bình kín chứa 0,04 mol C2H2; 0,06 mol H2, một ít Ni.
Nung → hhY.
hhY + Br2 dư thì có 0,04 mol hhZ thoát ra. dZ/H2 = 4,5.
• Theo bảo toàn khối lượng: mC2H2 + mH2 = mbình brom tăng + mZ
→ mbình brom tăng = 0,04 x 26 + 0,06 x 2 - 0,04 x 9 = 0,8 gam


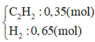
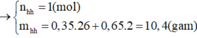
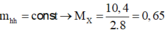

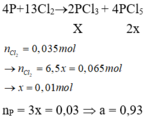
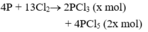
Đáp án A
Trong một bình kín chứa 0,35 mol C2H2; 0,65 mol H2 và một ít bột Ni.
Nung bình → hhX có dX/H2 = 8.
Theo BTKL: mhhX = mhh ban đầu = 0,35 x 26 + 0,65 x 2 = 10,4 gam
→ nhhX = 10,4 : 16 = 0,65 mol.
→ nH2phản ứng = nhh ban đầu - nX = 0,35 + 0,65 - 0,65 = 0,35 mol.
Ta có: nπ trước phản ứng = 2 x nCH≡CH = 2 x 0,35 = 0,7 mol.
→ nπ dư = nπ trước phản ứng - nH2 = 0,7 - 0,35 = 0,35 mol.
• Ta có nπ dư = 2 x nAgC≡CAg + nBr2
→ nBr2 = 0,35 - 2 x (12 : 240) = 0,25 mol