hòa tan 0,23 gam Na vào H2O dư thu được dung dịch X.Tính pH của dd X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$n_{Na} = \dfrac{4,6}{23} = 0,2(mol)$
$2Na + 2H_2O \to 2NaOH + H_2$
$n_{H_2} = \dfrac{1}{2}n_{Na} = 0,1(mol)$
$n_{NaOH} = n_{Na} = 0,2(mol)$
Sau phản ứng :
$m_{dd} = 4,6 + 120,6 - 0,1.2 = 125(gam)$
$C\%_{NaOH} = \dfrac{0,2.40}{125}.100\% =6,4\%$
2Na+ 2H2O→ 2NaOH+ H2
(mol) 0,2 0,2 0,2 0,1 nNa=\(\dfrac{m}{M}=\dfrac{4,6}{23}=0,2\)(mol)
\(n_{H_2O}=\dfrac{m}{M}=\dfrac{120,6}{18}=6,7\)(mol)
Xét tỉ lệ:
Na H2O
\(\dfrac{0,2}{2}\) < \(\dfrac{6,7}{2}\)
=> Na phản ứng hết, nước dư
\(m_{H_2}\)=n.M=0,1.2=0,2(g)
mdd sau phản ứng = mNa+ \(m_{H_2O}\)-\(m_{H_2}\)
= 4,6 +120,6 -0,2= 125(g)
mNaOH=n.M= 0,2.40=8(g)
C%NaOH=\(\dfrac{8}{125}.100\%=0,064\%\)

Chọn đáp án B
Nhận xét nhanh
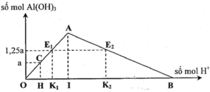
+ Vì hỗn hợp Na và Al (tỉ lệ mol 1:1) nên dung dịch X chỉ có NaAlO2.
+ Vì lượng HCl tăng 1,5 lần mà lượng kết tủa tăng chưa đến 1,5 lần.Nên lần 1 kết tủa chưa cực đại và lần 2 kết tủa đã bị tan 1 phần.
Ta có
![]()
![]()
Với thí nghiệm 2
![]()
![]()
![]()
![]()

Đáp án A
nOH- = 2nH2 = 0,06mol
=> nFe(OH)3 = 0,02mol
=> m = 2,14g

Đáp án A
nOH- = 2nH2 = 0,06mol
=> nFe(OH)3 = 0,02mol
=> m = 2,14g

Đáp án C
Các phản ứng: Na + H2O → NaOH + ½ H2
2NaOH + H2SO4 → Na2SO4 + 2H2O
nH2SO4 = 0,1.1 = 0,1 mol
Theo các phản ứng: nNa = nNaOH = 2nH2SO4 = 0,2 mol
=> mNa = m = 23.0,2 = 4,6g

\(n_{NaCl}=\dfrac{1,17}{58,5}=0,02\left(mol\right)\\ n_{BaCl_2}=\dfrac{2,08}{208}=0,01\left(mol\right)\\ \left[Na^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\ \left[Ba^{2+}\right]=\dfrac{0,01}{0,1}=0,1\left(M\right)\\ \left[Cl^-\right]=\dfrac{0,02+0,01.2}{0,1}=0,4\left(M\right)\)

Đáp án D
Do VH2 thu được ở 2 thí nghiệm khác nhau
⇒ Al dư ở thí nghiệm 1.
Đặt nNa = x; nAl = y.
● Xét thí nghiệm 1: Na → NaOH → NaAlO2.
⇒ nAl phản ứng = nNa = x.
Bảo toàn electron:
x + 3x = 2 × 0,4 ⇒ x = 0,2 mol.
● Xét thí nghiệm 2: Do NaOH dư
⇒ Al tan hết. Bảo toàn electron:
x + 3y = 2 × 0,55 ⇒ y = 0,3 mol.
||► m = 0,2 × 23 + 0,3 × 27 = 12,7(g).