cho nổ 1 hỗn hợp gồm 1 mol hidro và 2 mol khí oxi <dktc> . Chất nào còn dư
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Khi cho Al phản ứng với NaOH hoặc HCl thì số mol H2 thu được là như nhau:
nH2= 0,3 mol ⇒ nAl = 0,2 mol
Từ đó suy ra nH2 do Fe tạo ra = 0,4 - 0,3 = 0,1 mol
⇒nFe = 0,1 mol ⇒ nAl đã phản ứng tạo Fe là 0,1 mol vì:

⇒∑n Al trong X = 0,1 + 0,2 = 0,3mol

2H2 + O2 --to--> 2H2O
Xét \(\dfrac{0,2}{2}>\dfrac{0,08}{1}\) => H2 dư, O2 hết
=> Hiệu suất phản ứng tính theo O2
\(n_{O_2\left(pư\right)}=\dfrac{0,08.75}{100}=0,06\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
____0,12<-0,06------>0,12
=> \(Y\left\{{}\begin{matrix}m_{O_2}=\left(0,08-0,06\right).32=0,64\left(g\right)\\m_{H_2}=\left(0,2-0,12\right).2=0,16\left(g\right)\\m_{H_2O}=0,12.18=2,16\left(g\right)\end{matrix}\right.\)

Đáp án B
Ta có:
![]()
mCu = 0,7m (g)
Vì Fe phản ứng trước Cu và sau khi phản ứng còn 0,75m (g) chất rắn → Cu chưa phản ứng 0,7m
Fe dư 0,75m - 0,7m = 0,05m → mFe pư = 0,2m - 0,05m = 0,25m (g)
Fe dư → Chỉ tạo muối Fe(NO3)2
HNO3 hết (Lưu ý chỉ H+ hết, NO3- còn trong muối).
Quá trình nhường electron:

Quá trình nhận electron:
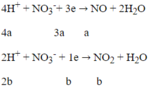
Áp dụng định luật bảo toàn electron:
![]()
→ m = 50,4

Đáp án B
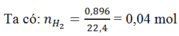
Gọi: nNa = x mol ⇒ nAl = 2x mol
Phản ứng:
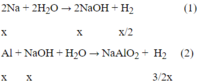
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1), (2)
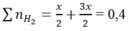
![]()
⇒mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒mAl = 0,2.27 = 5,4 (g)

Đáp án C
Ta có: nH2= 0,04 mol
Gọi: nNa = x mol " nAl = 2x mol
Phản ứng:
2Na + 2H2O → 2NaOH + H2 (1)
x x x 2
Al + NaOH + H2O → NaAlO2 + 3 2 H2 (2)
x x 3 2 x
Sau các phản ứng còn m(g) chất rắn không tan, đó là khối lượng của Al dư.
Theo phản ứng (1) ; (2)

⇒ mAl ban đầu = 2x = 0,2.2 = 0,4 mol
Mà: nAl phản ứng = nNaOH = x = 0,2 mol ⇒ nAl dư = 0,4 - 0,2 = 0,2 mol
⇒ mAl = 0,2.27 = 5,4 (g)

a, Giả sử: \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{SO_2}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow x+y=\dfrac{0,224}{22,4}=0,01\left(1\right)\)
Mà: \(\overline{M}_A=56\Rightarrow44x+64y=56.0,01\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,004\left(mol\right)\\y=0,006\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%n_{CO_2}=\dfrac{0,004}{0,01}.100\%=40\%\\\%n_{SO_2}=60\%\end{matrix}\right.\)
BTNT C và S, có: \(\left\{{}\begin{matrix}n_{Na_2CO_3}=n_{CO_2}=0,004\left(mol\right)\\n_{Na_2SO_3}=n_{SO_2}=0,006\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{0,004.106}{0,004.106+0,006.126}.100\%\approx35,9\%\\\%m_{Na_2SO_3}\approx64,1\%\end{matrix}\right.\)
b, Ta có: \(n_{HCl}=0,05.0,2=0,01\left(mol\right)\)
PT: \(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
____0,005_______0,01 (mol)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3+H_2O\)
_0,004______0,004 (mol)
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3+H_2O\)
_0,006_____0,006 (mol)
\(\Rightarrow n_{Ba\left(OH\right)_2}=0,015\left(mol\right)\)
\(\Rightarrow C_{M_{Ba\left(OH\right)_2}}=\dfrac{0,015}{1}=0,015M\)
Bạn tham khảo nhé!






Nguyễn Kim Tuyến Bên trên là lời giải chi tiết nhất rồi bạn nhé! Bạn còn chỗ nào không hiểu nhỉ?
2H2+O2\(\underrightarrow{t^0}\)2H2O
lập tỉ lệ :\(\dfrac{1}{2}<\dfrac{2}{1}\)
=> oxi dư