Chất A tạo bởi A nguyên tử X và b nguyên tử Y . Mỗi phân tử A gồm 3 nguyên tử ; phân tử khối của A bằng 160 đvC . Hạt nhân nguyên tử Y có số hạt mang điện bằng số hạt mang điện bằng số hạt không mang điện; hạt nhân nguyên tử X có số hạt mang điện bằng 82,857% số hạt không mang điện. Số hạt mang điện của 2 nguyên tử X,Y hơn kém nhau 26 hạt . Xác định công thức của phân tử hợp chất
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTHH: XaYb
=> \(\left\{{}\begin{matrix}a+b=3\\a.NTK_X+b.NTK_Y=160\Rightarrow a\left(p_X+n_X\right)+b\left(p_Y+n_Y\right)=160\left(1\right)\end{matrix}\right.\)
Hạt nhân Y có số hạt mang điện bằng số hạt không mang điện
=> pY = nY
Hạt nhân nguyên tử X có số hạt mang điện bằng 82,857% số hạt không mang điện
=> pX = nX.82,857%
(1) => a.1,82857.nX + 2.b.nY = 160 (2)
Do số hạt mang điện của 2 nguyên tử X, Y hơn kém nhau 26 hạt
=> \(\left[{}\begin{matrix}2p_X-2p_Y=26\Rightarrow1,65714p_X-2n_Y=26\left(3\right)\\2p_Y-2p_X=26\Rightarrow2n_Y-1,65714n_X=26\left(4\right)\end{matrix}\right.\)
TH1: a = 1; b = 2
=> CTHH: XY2
(2) => 1,82857.nX + 4.nY = 160 (5)
(3)(5) => \(\left\{{}\begin{matrix}n_X=41\Rightarrow p_X=34\left(Se\right)\\n_Y=21\Rightarrow p_Y=21\left(Sc\right)\end{matrix}\right.\) => CTHH: SeSc2 (Loại)
(4)(5) => \(\left\{{}\begin{matrix}n_X=21\Rightarrow p_X=17\left(Cl\right)\\n_Y=30\Rightarrow p_Y=30\left(Zn\right)\end{matrix}\right.\) => CTHH: ClZn2 (Loại)
TH2: a = 2; b = 1
=> 3,65714.nX + 2nY = 160 (6)
(3)(6) => \(\left\{{}\begin{matrix}n_X=35\Rightarrow p_X=29\left(Cu\right)\\n_Y=16\Rightarrow p_Y=16\left(S\right)\end{matrix}\right.\) => CTHH: Cu2S (chọn)
(4)(6) => \(\left\{{}\begin{matrix}n_X=25\Rightarrow p_X=21\left(Sc\right)\\n_Y=34\Rightarrow p_Y=34\left(Se\right)\end{matrix}\right.\) => CTHH: Sc2Se (Loại)
Vậy CTHH là Cu2S
Phân tử A gồm 3 nguyên tử => a+b=3 (1)
Gọi u,k lần lượt bằng số hạt không mang điển của X,Y (u,k:nguyên, dương)
=> Số hạt trong hạt nhân 1 nguyên tử X: u+ 0,82857u =1,82857u (hạt)
Số hạt trong hạt nhân 1 nguyên tử Y: k + k = 2k(hạt)
=> 1,82857u+ 2k= 160 (2)
Mặt khác: 2.0,82857u - 2k= 26 (3)
(2), (3) lập hpt giải hệ: u=53,4 ; k=31,2
- Lập bảng xét giá trị a,b sau đó thế vào (2):
| a | 1 | 2 |
| b | 2 | 1 |
| PTK | 169,2 | 276 |
Anh không biết tới đây anh sai đâu không nhưng số xấu quá em.(Ban đầu anh nghĩ PTK 160 mà 3 nguyên tử là Cu2O nhưng qua tính toán thì không phải rồi...)

a) Công thức phân tử của A là: \(X_2O_3\)
\(\Rightarrow2M_X+16\times3=160\\\Leftrightarrow M_x=56\)
b) \(M_B=0.5M_A=0.5\times160=80\left(dvc\right)\)
Công thức phân tử của B là: \(YO_3\)
\(\Rightarrow M_Y+16\times3=80\\ \Leftrightarrow M_Y=32\)

Gọi công thức của A là H 3 X O y (vì nhóm X O y hóa trị III nên theo quy tắc hóa trị ta xác định được phân tử có 3 nguyên tử H)
Phân tử khối của H 2 S O 4 : 2 + 32 + 16.4 = 98 (đvC)
Vì A nặng bằng phân tử H 2 S O 4 nên PTK của A là 98 đvC
Theo đề bài, ta có khối lượng của nguyên tố oxi trong hợp chất là:
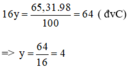
→ có 4 nguyên tử oxi trong hợp chất A.
Vậy nguyên tử khối của X là: 98 – (3 + 64) = 31 (đvC)

a,Gọi CTHH của hợp chất A là X2Y3
Ta có: \(\dfrac{X}{7}=\dfrac{Y}{3}=\dfrac{X+Y}{7+3}=\dfrac{160}{10}=16\)
\(\Rightarrow2M_X=7.16\Leftrightarrow M_X=56;3M_Y=3.16\Leftrightarrow M_Y=16\)
⇒ X là sắt (Fe),Y là oxi (O)
b, CTHH của A là Fe2O3

bài 1:a) ta có A= 2.X+3.O=2X+3.16=> 2X=160-3.16=112=> X=56
X có nguyên tử khối là 56 => X là sắt (Fe)
b) Phân tử khối của B là B=A-0,5A=0,5A=0,5.160=80
mặt khác B=Y+3.O=> Y=B-3.O=80-3.16=32
=> Y có phân tử khối là 32=> Y là lưu huỳnh (S)

bài 1:a) ta có A= 2.X+3.O=2X+3.16=> 2X=160-3.16=112=> X=56
X có nguyên tử khối là 56 => X là sắt (Fe)
b) Phân tử khối của B là B=A-0,5A=0,5A=0,5.160=80
mặt khác B=Y+3.O=> Y=B-3.O=80-3.16=32
=> Y có phân tử khối là 32=> Y là lưu huỳnh (S)

Hợp chất X : $R_2O_5$(lập CTHH dựa quy tắc hóa trị)
$M_X = 2R + 5O = 2R + 16.5 = 142\ đvC \Rightarrow R = 31(đvC)$
Vậy R là nguyên tố Photpho, CTHH X : $P_2O_5$
Hợp chất Y : $A_2(SO_4)_a$(lập CTHH dưa quy tắc hóa trị )
$M_Y = 2A + 96a =142 : 0,355 = 400\ đvC$
Với a = 1 thì A = 152 - loại
Với a = 2 thì A = 104 - loại
Với a = 3 thì A = 56 (Fe)
Vậy A là nguyên tố Fe, CTHH Y : $Fe_2(SO_4)_3$
Gọi cthh của A dưới dạng XaYb
Vì trong A gồm có 3 nguyên tử nên cthh của A gồm 2 loại: XY2 hoặc X2Y
Gọi proton,notron,electron của X là lần lượt là p,n,e
Gọi proton,notron,electron của Y là lần lượt của a,s,d
Theo đề,ta có: _a = s
_p = 82,857% n \(\rightarrow\) n = 82,857p/100
_(p + e) - (a + s) = 26 (p=e;a=s)
\(\rightarrow\) 2p - 2a= 26 (1)'
Giả sử cthh của A có dạng XY2
\(\rightarrow\)M A = M X + 2M Y =(p+e) + 2(a+s)
= (p+ 82,857p/100) + 2.2a
= 2,207 p + 4a = 160 (2)
Giải (1)' và (2) \(\rightarrow\)p = 34,a= 21
Mà không có nguyên tố nào có số proton = 34 hay 21 \(\rightarrow\)Cthh của A có dạng X2Y
\(\rightarrow\) M A = 2 M X + M Y
= 2(p+ 82,857p/100) + 2a
=4,414p +2a = 160 (1)
Giải (1) và (1)'\(\rightarrow\)
p = 64 vậy X là Cu, a = 32 vậy Y là S
Vậy CTHH là: Cu2S