Biết rằng nguyên tố Y có khối lượng nguyên tử = 5,31*10-23(g). Hãy xác định nguyên tử khối của Y
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a
Số nguyên tử X có khối lượng bằng 14,2 gam là: \(1,2.10^{23}.2=2,4.10^{23}\) (nguyên tử)
\(\Rightarrow n_X=\dfrac{2,4.10^{23}}{6.10^{23}}=0,4\left(mol\right)\)
\(M_{phân.tử.X}=\dfrac{14,2}{0,4}.2=71\left(g/mol\right)\)
b
\(M_{nguyên.tử.khối.X}=\dfrac{71}{2}=35,5\left(đvC\right)\)
X là nguyên tố Cl (Clo)

Gọi công thức của A là H 3 X O y (vì nhóm X O y hóa trị III nên theo quy tắc hóa trị ta xác định được phân tử có 3 nguyên tử H)
Phân tử khối của H 2 S O 4 : 2 + 32 + 16.4 = 98 (đvC)
Vì A nặng bằng phân tử H 2 S O 4 nên PTK của A là 98 đvC
Theo đề bài, ta có khối lượng của nguyên tố oxi trong hợp chất là:
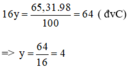
→ có 4 nguyên tử oxi trong hợp chất A.
Vậy nguyên tử khối của X là: 98 – (3 + 64) = 31 (đvC)

\(n_A=\dfrac{0,6.10^{23}}{6.10^{23}}=0,1(mol)\\ \Rightarrow M_A=\dfrac{5,6}{0,1}=56(g/mol)\)
Vậy A là sắt (Fe)
\(n_A=\dfrac{0,6.10^{23}}{6.10^{23}}=0,1\left(mol\right)\)
=> \(M_A=\dfrac{5,6}{0,1}=56\left(g/mol\right)\)
=> A là Fe(sắt)

Bài 1 :
Do NTKchất (đvC) = mchất đó : (1,66*10-24)
=> NTKx = (6,6553*10-23 ) : (1,66 * 10-24)
=> NTKx = 40 (đvC)
=> X là nguyên tố Canxi ( Ca)

2. Lấy NTK của O và S nhân với 1/12 khối lượng của C(có ghi trong sgk)
5. Ta có:
PTK của Y= 4X+ 10H=29x2(PTK của PT H là 2)
=>4X+10x1=48
=>4X=38
=>X=...
=>
Nguyên tử khối của Y:NTKY=\(\dfrac{5,31.10^{-23}}{1,6605.10^{-24}}\)=32(đvC)
giải rõ ra đi