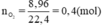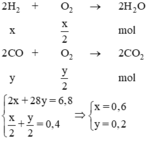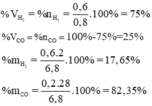vẽ biểu dồ so sánh khối lượng của 11,2g của oxi, hidro, clo, amoniac ( thể tích đo ở đktc)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


đề là 11,2 lít nha
Ta có số mol của các chất khí trên trong 11,2 lít mỗi khí là :
n = 22,4 : 11,2 = 2 (mol)
=> mO2 = 2 * 32 = 64 (g)
=> mH2 = 2 * 2 = 4 (g)
=> mCl2 = 35,5 * 2 = 71 (g)
=> mNH3 = 17 * 2 = 34 (g)
Ta có biểu đồ so sánh khối lượng :
Khối lượng(g) 10 20 30 40 50 60 70 0 O2 H2 Cl2 NH3 64 4 71 34 tên chất

Coi $n_A = 1(mol) \Rightarrow m_A = 1.2.13,5 = 27(gam)$
$m_{NH_3} + m_{O_2} + m_{N_2} = 27$
$\Rightarrow \dfrac{7}{8}m_{O_2} + m_{O_2} + \dfrac{3}{6} (m_{O_2} + m_{NH_3} ) = 27$
$\Rightarrow \dfrac{7}{8}m_{O_2} + m_{O_2} + \dfrac{3}{6} (m_{O_2} + \dfrac{7}{8}m_{O_2} ) = 27$
$\Rightarrow \dfrac{45}{16}m_{O_2} = 27 \Rightarrow m_{O_2} = 9,6(gam)$
Suy ra:
$m_{NH_3} = 8,4 ; m_{N_2} = 9$
Suy ra : $n_{O_2} = 0,3(mol) ; n_{NH_3} = \dfrac{42}{85}(mol)$
$\%V_{O_2} = \dfrac{0,3}{1}.100\% = 30\%$
$\%V_{NH_3} = 49,41\%$
$\%V_{N_2} = 20,59\%$

n
H
2
=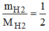 = 0,5(mol)
= 0,5(mol)
n
O
2
=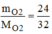 = 0,75(mol)
= 0,75(mol)
n
N
2
=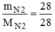 = 1(mol)
= 1(mol)
n
C
O
2
=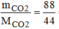 =2(mol)
=2(mol)
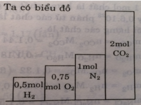
Tỉ lệ thể tích cũng chính là tỉ lệ về số mol nên ta có biểu đồ sau:

\(n_{Fe}=\dfrac{m}{M}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
\(0,2\) → \(\dfrac{2}{15}\) → \(\dfrac{1}{15}\) ( mol )
a) \(m_{Fe_3O_4}=n.M=\dfrac{1}{15}.\left(56.3+16.4\right)=\dfrac{232}{15}\left(g\right)\)
b) \(V_{O_2}=n.22,4=\dfrac{2}{15}.22,4=\dfrac{224}{75}\left(l\right)\)