giải gúp em bài 8 thui
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



13 - (2x + 5) = 21 + (22-x)
<=> 13 - 21 = (22-x) + (2x + 5)
=> -8 = 22 - x +2x +5
=> -8 = x + 27
=> x = -8 - 27
=> x = -35.
13-(2x +5) = 21 + (22-x)
=>13 - 2x - 5 = 21 + 22 - x
=>8 - 2x = 43 - x
=>43 - x - (8 - 2x) = 0
=>43 - x - 8 + 2x = 0
=>35 + 2x - x = 0
=>35 + x = 0
=> x = 0 - 35
=> x = - 35

Bài 5:
a: \(\dfrac{8}{15}:x=\dfrac{-20}{21}\)
\(\Leftrightarrow x=\dfrac{-8}{15}\cdot\dfrac{21}{20}=\dfrac{-168}{300}=\dfrac{-14}{25}\)
c: \(x:\left(-4\dfrac{2}{7}\right)=-4\dfrac{1}{5}\)
\(\Leftrightarrow x=\dfrac{-21}{5}\cdot\dfrac{-30}{7}=3\cdot6=18\)

Bài 1:
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: nH2 = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: VH2= 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
Bài 2:
a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
Số mol của S tham gia phản ứng:
nS = 16/32 = 0,05 mol
Theo phương trình hóa học, ta có: nSO2 = nS = nO2 = 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
VSO2= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
VO2 = 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 VO2 = 5 . 1,12 = 5,6 lít
Bài 1 :
a) PTPU
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (lít)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)
Bài 2 :
a) Phương trình hóa học của S cháy trong không khí:
S + O2 to→→to SO2
b) Số mol của S tham gia phản ứng:
nS = 1,6321,632 = 0,05 mol
- Theo phương trình hóa học, ta có: nSO2nSO2 = nS = 0,05 mol
Thể tích khí sunfurơ sinh ra ở đktc là:
VSO2VSO2 = 22,4 . 0,05 = 1,12 (lít)
- Theo phương trình hóa học, ta có: nO2nO2 = nS = 0,05 mol
Thể tích khí oxi cần dùng ở đktc là:
VO2VO2 = 22,4 . 0,05 = 1,12 (lít)
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần dùng ở đktc là:
Vkk = 5VO2VO2 = 5 . 1,12 = 5,6 (lít)

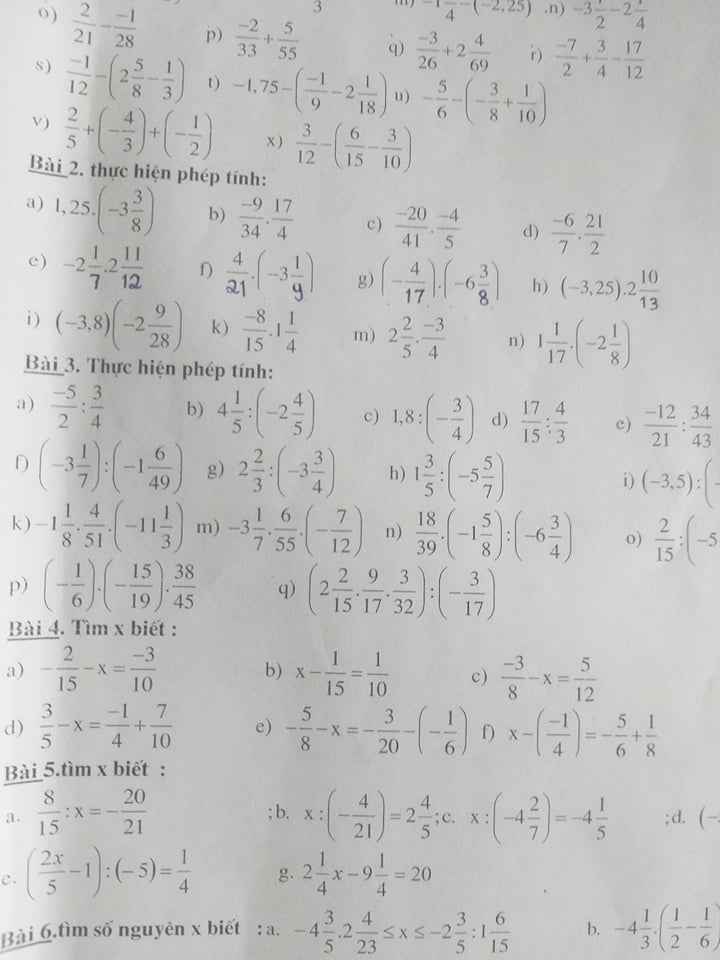 Hơi nhiều bài m.n giải gúp mình nha
Hơi nhiều bài m.n giải gúp mình nha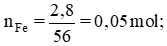
Bài 8 :
Tóm tắt
R1 = 20Ω
U = 3,2V
a) I1 = ?
b) R2 = ?
a) I1 = \(\dfrac{U}{R_1}=\dfrac{3,2}{20}=0,16\left(A\right)\)
b) Có : I2 = 0,8 . I1
= 0,8 . 0,16
= 0,128 (A)
I2 = \(\dfrac{U}{R_2}\Rightarrow R_2=\dfrac{U}{I_2}=\dfrac{3,2}{0,128}=25\) (Ω)
Chúc bạn học tốt