Cho 11,2l H2 (đktc) tác dụng với 0,45 mol Cl2 thu được 0,6 mol HCl . Tính hiệu suất phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Hỗn hợp rắn sau pư gồm: Fe và FeCl3.
Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
BT e, có: \(2n_{Fe}=2n_{H_2}\Rightarrow n_{Fe}=0,1\left(mol\right)\)
BTNT Fe, có: \(n_{FeCl_3}=n_{Fe\left(OH\right)_3}=0,03\left(mol\right)\) = nFe (pư)
BTNT Fe, có: nFe (ban đầu) = nFe + nFeCl3 = 0,13 (mol)
\(\Rightarrow H\%=\dfrac{0,03}{0,13}.100\%\approx23,077\%\)

Chọn đáp án B
► Xét phần 1: Y + NaOH → H2. Mặt khác, phản ứng xảy ra hoàn toàn ⇒ Al dư.
nAl dư = 0,15 ÷ 1,5 = 0,1 mol. Phần không tan T là Fe ⇒ nFe = nH2 = 0,45 mol.
Lần lượt bảo toàn nguyên tố Oxi và Fe ⇒ nAl2O3 = 0,2 mol.
● GIẢ SỬ phần 1 tác dụng với HCl thì nH2 = 0,1 × 1,5 + 0,45 = 0,6 mol.
||⇒ phần 2 gấp 1,2 ÷ 0,6 = 2 lần phần 1 ⇒ lượng ban đầu gấp 3 lần phần 1.
► m = 3 × (0,1 × 27 + 0,2 × 102 + 0,45 × 56) = 144,9(g) ⇒ chọn B.
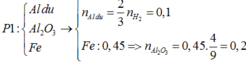
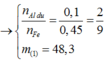
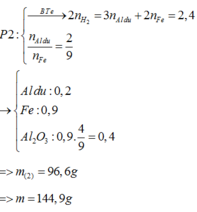




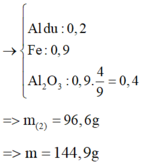
H2+Cl2-->2HCl
Số mol của H2 là
n=V/22,4
=11,2/22,4=0,5(mol)
Khối lượng của H2 là
m=n.M=0.5.2=1(g)
K/lượng của Cl2 là
m=n.M=0,45.71=31,95(g)
Áp dụng định luật bảo toàn k/lượng ta có:
mHCl=mH2+mCl2
=1+31,95=32,95 g
K/lượng của HCl thực tế là
m=n.M=0,6.36,5=21,9(g)
Hiệu suất phản ứng là
H=(m tt/m ct).100%
=(21,9/32,95).100%
=66,464%