trong phòng thí nghiệm có 6 chất: Na2CO3; BaCl2; MgSO4; NaCl; AlCl3; KOH để pha chế thành 3 dung dịch A; B; C. mỗi dung dịch chứa 2 chất và có đặc điểm: A có pH <7; B có pH = 7; C có pH >7. xác định thành phần của A; B; C. có thể dùng H2SO4 để nhận biết 3 dung dịch đó không? giải thích và viết phương trình
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Lần lượt cho 3 chất vào 3 ống nghiệm đựng dung dịch HCl, nếu chất nào tan và có khí bay ra là Na 2 CO 3 , BaCO 3 và chất nào tan mà không có khí bay ra là NaCl.
Na 2 CO 3 + 2HCl → 2NaCl + CO 2 + H 2 O (1)
BaCO 3 + 2HCl → Ba Cl 2 + CO 2 + H 2 O (2)
- Sau đó hoà tan một ít Na 2 CO 3 và BaCO 3 vào nước. Chất nào tan trong nước là Na 2 CO 3
Chất không tan trong nước là BaCO 3

Na2CO3 + 2HCl →2NaCl + H2O + CO2
Na2CO3 + CaCl2 →2NaCl + CaCO3
NaHCO3 + HCl → NaCl + H2O + CO2
Dung dịch trong lọ C vừa tạo kết tủa, vừa tạo khí khi tác dụng với 2 dung dịch khác nên dung dịch trong lọ C là Na2CO3.
Dung dịch trong lọ D tạo khí khi tác dụng với 2 dung dịch khác nên dung dịch trong lọ D là HCl
Dung dịch trong lọ A tác dụng với dung dịch C tạo kết tủa nên dung dịch trong lọ A là CaCl2.
Dung dịch trong lọ B tác dụng với dung dịch D tạo khí nên dung dịch trong lọ B là NaHCO3.

2KMnO4-to>MnO2+K2MnO4+O2
2H2O-đp->2H2+O2
2Cu+O2-to>2CuO
3Fe+2O2-to>Fe3O4
4Al+3O2-to>2Al2O3
\(MnO_2:2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\\ CuO:2Cu+O_2\underrightarrow{t^o}2CuO\\ Fe_3O_4:3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\\ Al_2O_3:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)

2KMNO4-to>K2MnO4+MnO2+O2
2H2O-đp->2H2+O2
2Cu+O2-to>2CuO
3Fe+2O2-to>Fe3O4
4Al+3O2-to>2Al2O3
phân Hủy KMnO4 tạo ra MnO2
pthh : 2KMnO4 -t-> K2MnO4 + MnO2 + O2
lấy 1 nửa O2 vừa dùng được tác dụng với Fe
pthh : 3Fe + 2O2 -t-> Fe3O4
lấy phần còn lại tác dụng với Al
pthh : 4Al + 3O2 -t-> 2Al2O3

Đáp án A
Y là chất rắn có màu đen, suy ra Y có thể là : CuO, Ag2O, FeO, MnO2,... Tuy nhiên đây là phản ứng điều chế khí nên Y phải là MnO2 và X là khí Cl2.
Phương trình phản ứng :
![]()

Đáp án C
O2, CO2 là hai khí ít tan trong nước
N2 không tan trong nước
NH3 là khí tan tốt trong nước (1 lít nước ở 200C có thể hòa tan tối đa 800 lít NH3)

Làm Cách khác nhé :
+Cho nhúm quỳ tím ,và nhỏ nước :
- Chất tan , làm quỳ chuyển xanh là:Na2CO3
- Chất tan l, ko hiện tượng là NaCl
- Chất còn lại là Al2O3, CaCO3
+Ta nhỏ H2SO4
-Chất td , có khí thoát ra và kết tủa là CaCO3
-Chất tan là Al2O3
CaCO3+H2SO4->CaSO4+H2O+CO2
Al2O3+6HCl->2AlCl3+3H2O
Tham khảo :
trích mẫu thử
cho vào mỗi mẫu thử 1 mẩu quì tím
+ mẫu thử làm quì tím chuyển sang màu đỏ là HCl
+ 3 mẫu thử còn lại không làm quì tím chuyển màu
- cho vài giọt dd HCl vừa nhận biết được vào 3 mẫu thử còn lại
+ có khí thoát ra là Na2CO3
Na2CO3+ 2HCl→→ 2NaCl+ CO2↑↑+ H2O
+ 2 mẫu thử còn lại không phản ứng
- cho vài giọt dd Na2CO3 vừa nhận biết được vào 2 mẫu thử còn lại
+ có kết tủa là CaCl2
CaCl2+ Na2CO3→→ 2NaCl+ CaCO3↓↓
còn lại là NaCl

\(a,Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ b,CO_2+H_2O\rightarrow H_2CO_3\\ c,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ C+O_2\underrightarrow{t^o}CO_2\)
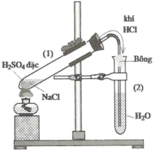
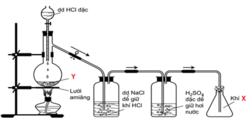
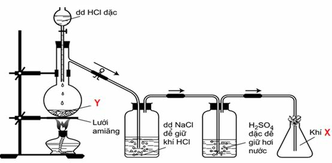
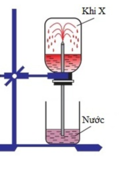
A: H2CO3, HCL
pt : NaCl + H2O điện phân dung dịch có màng ngăn -> NaOH + H2 + Cl2
H2 + Cl2 ánh sáng -> HCl ( sục khí HCL vào nước thu dd Axit )
HCl + Na2CO3 -> NaCl + H2O + CO2
H2O + CO2 -> <- H2CO3
B: NaAlO2 , MgCl2
pt : BaCl2 + MgSO4 -> BaSO4 + MgCl2
AlCl3 + NaOH -> NaAlO2 + H2O
C: Ba(OH)2, NaOH :
pt: NaCl + H2O điện phân dung dịch -> NaOH + H2 + Cl2
BaCl2 + H2O điện phân dung dịch -> Ba(OH)2 + H2 + Cl2
mình chỉ giải được đến đây, với kbt đúng không :v
cảm ơn bạn