Cho 2 hợp chất sau: CO2 và NH3
a) Viết công thức Lewis và công thức cấu tạo của 2 hợp chất trên.
b) Hợp chất nào tan trong nước, hợp chất nào không tan trong nước? Giải thích cụ thể.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Y có số hiệu nguyên tử là 8 => Y là oxi
=> cấu hình electron là: \(1s^22s^22p^4\)
X có số hiệu nguyên tử là 11 => X là natri
=> cấu hình electron là: \(1s^22s^22p^63s^1\)
b.O + 2e → O2-
2Na \(\rightarrow\) 2Na\(^{1+}\)+2e
=> \(2Na^{1+}+O^{-2}\rightarrow Na_2O\)

a. Số mol khí N2 là: \(\dfrac{0,336}{22,4}=0,015\left(mol\right)\)
Số phân tử N2 là: 0,015 x 6.1023 = 9.1021 (phân tử)
Số nguyên tử N là: 2x9.1021=18.1023 (nguyên tử)
b. Khối lượng N2 là: 0,015x28 = 0,42 (g)
c. Thể tích khí N2 ở đk thường là: \(\dfrac{0,336}{24}=0,014\left(mol\right)\)
Thể tích khí N2 ở đk chuẩn là: \(\dfrac{0,336}{24,7}=0,0136\left(mol\right)\)
d. Số mol H2 là: \(\dfrac{1}{2}=0,5\left(mol\right)\)
Khối lượng mol của hỗn hợp khí A: \(M_A=\dfrac{0,5x2+0,015x28}{0,5+0,015}=\dfrac{1,42}{0,515}\simeq2,757\)
+ Tỷ khối của hỗn hợp khí A với Mêtan:
\(M_A=\dfrac{1,42}{0,515x16}\simeq0,17\)
+ Tỷ khối của hỗn hợp khí A với không khí:
\(M_A=\dfrac{1,42}{0,515x29}\simeq0,095\)

Gọi kim loại cần tìm là R
\(2R+3Cl_2\rightarrow2RCl_3\)
\(n_R=\dfrac{8,1}{M_R}\) (1)
\(n_{RCl_3}=\dfrac{40,05}{M_R+106,5}\) (2)
Theo PTHH: \(n_R=n_{RCl_3}\) (3)
Từ (1),(2) và (3) suy ra
\(\dfrac{8,1}{M_R}=\dfrac{40,05}{M_R+106,5}\)
\(\Rightarrow M_R=27\)
Vậy R là nhôm ( Al)

Các nguyên tử khí hiếm đều có cấu hình electron lớp ngoài cùng đặc biệt bền vững: ns2np6ns2np6 (trừ heli có cấu hình 1s21s2). Các nguyên tử khí hiếm rất khó tham gia phản ứng hóa học. Trong tự nhiên, các khí hiếm đều tồn tại ở dạng nguyên tử (hay còn gọi là phân tử một nguyên tử) tự do (nên còn gọi là các khí trơ).

a) \(\%N=1005-36,36\%=63,64\%\)
Ta có: \(\dfrac{m_N}{m_O}=\dfrac{\%N}{\%O}\)
=> \(\dfrac{14x}{16y}=\dfrac{63,64}{36,36}\Leftrightarrow\dfrac{x}{y}=\dfrac{63,64}{36,36}.\dfrac{16}{14}=\dfrac{2}{1}\)
=> CTHH của chất có dạng \(\left(N_2O\right)_n\)
Mà \(M_{\left(N_2O\right)_n}=44\left(g/mol\right)\)
=> \(n=\dfrac{44}{44}=1\left(TM\right)\)
=> Chất là N2O
b) Gọi hóa trị của N là a, theo quy tắc hóa trị, ta có:
x.2 = 1.II => x = I
=> N có hóa trị I trong N2O
a. Công thức Lewis của CO2: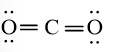
Công thức cấu tạo của CO2 là: O = C = O.
Công thức Lewis của NH3 là: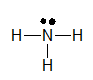
Công thức cấu tạo của NH3 là: \(H-N-H\)
\(|\)
H
b. Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử