Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

NaBr + AgNO3 \(\rightarrow\)AgBr + NaNO3
NaCl + AgNO3 \(\rightarrow\) AgCl + NaNO3
\(C_M=0,5M\Rightarrow n_{AgNO_3}=0,025\left(mol\right)\)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
\(\Rightarrow x=9,0557.10^{-3};y=0,01594\)
\(\Rightarrow C\%=\frac{0,594.58,5}{50}.100\%=1,865\%\)
NaBr + AgNO3 →→AgBr + NaNO3
NaCl + AgNO3 →→ AgCl + NaNO3
CM=0,5M⇒nAgNO3=0,025(mol)CM=0,5M⇒nAgNO3=0,025(mol)
Gọi x, y lần lượt là số mol NaBr và NaCl
Ta có : x + y = 0,025
103x - 58,5y = 0
⇒x=9,0557.10−3;y=0,01594⇒x=9,0557.10−3;y=0,01594
⇒C%=0,594.58,550.100%=1,865%⇒C%=0,594.58,550.100%=1,865%

=
= 0, 025 mol
Phương trình hóa học của phản ứng:
NaBr + AgNO3 → AgBr↓ + NaNO3
X mol x mol x mol
NaCl + AgNO3 → AgCl↓ + NaNO3
Y mol y mol y mol
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Ta có hệ phương trình đại số:
Giải ra , ta có x = 0, 009 mol NaBr
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
C% = x 100% = 1,86%

- Tính acid phụ thuộc vào khả năng tách H của acid. Phân tử nào càng dễ tách H thì tính acid càng mạnh
- Trong nhóm halogen, từ F đến I có độ âm điện giảm dần
=> Khả năng liên kết H-X giảm dần
=> Khả năng tách H trong HX tăng dần
=> Tính acid tăng dần
=> Dung dịch HF có tính acid yếu nhất

Chọn đáp án A
m d d A g N O 3 = V.D = 50.1,0625 = 53,125 (gam)
ð m A g N O 3 = 53 , 125 . 8 100 = 4,25 (gam) => n A g N O 3 = 4 , 25 170 = 0,025 (mol)
Nồng độ % của 2 muối bằng nhau => Khối lượng 2 muối bằng nhau.
N a C l : x m o l N a B r : y m o l → x + y = 0 , 025 58 , 5 x = 103 y → x = 0 , 0159 y = 0 , 0091
ð
C
%
N
a
C
l
=
0
,
0159.58
,
5
50
.100% = 1,86%

Hai muối ban đầu có thể là Na2CO3 và CaCl2
PTHH: Na2CO3 + CaCl2 --> 2NaCl + CaCO3
Do dung dịch chỉ chứa muối NaCl
=> Phản ứng vừa đủ
=> \(\dfrac{n_{Na_2CO_3}}{n_{CaCl_2}}=\dfrac{1}{1}\)
Xét \(\dfrac{m_{Na_2CO_3}}{m_{CaCl_2}}=\dfrac{106.n_{Na_2CO_3}}{111.n_{CaCl_2}}=\dfrac{106}{111}\)

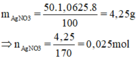
Phương trình hóa học của phản ứng:
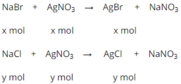
Biết nồng độ phần trăm của mỗi muối trong dung dịch bằng nhau và khối lượng dung dịch là 50g, do đó khối lượng NaCl bằng khối lượng NaBr.
Gọi nNaBr = x, nNaCl = y.
Theo pt: nNaBr = nAgNO3; nNaCl = nAgNO3
⇒ nNaBr + nNaCl = nAgNO3
Ta có hệ phương trình đại số: 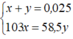
Giải ra, ta có x ≈ 0,009 mol
→ mNaBr = mNaCl = 103 x 0,009 = 0,927g
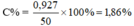

1: \(AgNO_3+NaI\rightarrow NaNO_3+AgI\downarrow\)
\(AgNO_3+NaCl\rightarrow NaNO_3+AgCl\downarrow\)
\(AgNO_3+NaBr\rightarrow NaNO_3+AgBr\downarrow\)
2: nếu xuất hiện kết tủa trắng thì ống nghiệm đó là NaCl
nếu xuất hiện kết tủa vàng nhạt thì ống nghiệm đó là NaBr
nếu xuất hiện kết tủa vàng đậm thì ống nghiệm đó là NaI
nếu ko xuất hiện kết tủa thì ống nghiệm đó là NaF

Tự cân bằng nhá!
a,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+Fe\rightarrow FeCl_3\\
FeCl_3+NaOH\rightarrow Fe\left(OH\right)_3+NaCl\\
NaCl+H_2SO_{4\left(dn\right)}\rightarrow Na_2SO_4+HCl\\
HCl+CuO\rightarrow CuCl_2+H_2O\\
CuCl_2+AgNO_3\rightarrow Cu\left(NO_3\right)_2+AgCl\)
b,
\(KMnO_4+HCl\rightarrow KCl+MnCl_2+Cl_2+H_2O\\ Cl_2+H_2\rightarrow HCl\\ HCl+Fe\left(OH\right)_3\rightarrow FeCl_3+H_2O\\ FeCl_3+AgNO_3\rightarrow Fe\left(NO_3\right)_3+AgCl\\ AgCl-as,t^o->Ag+Cl_2\\ Cl_2+NaBr\rightarrow NaCl+Br_2\\ Br_2+NaI\rightarrow NaBr+I_2\)
c, Giống câu b 3 pt đầu
\(HCl+Fe\left(OH\right)_2\rightarrow FeCl_2+H_2O\\
FeCl_2+AgNO_3\rightarrow Fe\left(NO_3\right)_2+AgCl\\
AgCl-as,t^o->Ag+Cl_2\)
d,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+Fe\rightarrow FeCl_3\\
FeCl_3+NaOH\rightarrow Fe\left(OH\right)_3+NaCl\\
Fe\left(OH\right)_3+H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+H_2O\)
e,
\(HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\
Cl_2+NaOH\rightarrow NaCl+NaClO+H_2O\\
NaCl+H_2SO_{4\left(dn\right)}\rightarrow Na_2SO_4+HCl\\
CuO+HCl\rightarrow CuCl_2+H_2O\\
CuCl_2+AgNO_3\rightarrow Cu\left(NO_3\right)_2+AgCl\\
AgCl-as,t^o->Ag+Cl_2\)
f,
\(MnO_2+HCl\rightarrow MnCl_2+Cl_2+H_2O\\ Cl_2+KOH-t^o->KClO_3+KCl+H_2O\\ KClO_3\rightarrow KCl+O_2\\ KCl+H_2SO_{4\left(dn\right)}\rightarrow K_2SO_4+HCl\\ HCl+MnO_2\rightarrow MnCl_2+Cl_2+H_2O\\ Ca\left(OH\right)_2+Cl_2\rightarrow CaCl_2+Ca\left(ClO\right)_2+H_2O\)

2Cl2 + 2H2O —> 4HCl + O2
Cl + 2Na —-> 2NaCl (nhiệt độ)
NaCl + AgNO3 —> AgCl + NaNO3
Bạn ở dưới sai sai thì phải:
2Na + Cl2 -> (t°) 2NaCl
NaCl + AgNO3 -> AgCl + AnNO3

\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\left(1\right)\\ m_{giảm}=m_{Br_2}-m_{Cl_2}\\ \Leftrightarrow n_{NaCl\left(1\right)}=n_{NaBr\left(1\right)}=\dfrac{13,35}{160-71}=0,15\left(mol\right)\\ \Rightarrow\%m_{NaBr}=\dfrac{103.0,15}{42,6}.100\approx36,268\%\\ \Rightarrow\%m_{NaCl}\approx63,732\%\)
Bổ sung:
\(C\%_{ddNaBr\left(trongA\right)}=\dfrac{0,15.103}{200}.100=7,725\%\\ C\%_{ddNaCl\left(trongA\right)}=\dfrac{42,6-0,15.103}{200}.100=13,575\%\)
=))
ummm......
cũng được!