Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

ta có nhôm (Al) tác dụng với axit sunfuric (H2SO4) thu được khi hidro( h2) và hợp chất nhôm sunfat Al2(SO4)3 nên có phương trình hóa học: Al + H2SO4 -> H2 + Al2(SO4)3
theo định luật bảo tồn khối lượng ta có :
m Al + m H2SO4 = m H2+ m Al2(SO4)3
Câu cuối tính m mình chưa biết tính cái chi nên không tính được.
chúc bạn học tốt nhé

`#\text{N073109}`
`a)`
PTHH: \(\text{Mg + 2HCl }\rightarrow\text{ MgCl}_2+\text{H}_2\)
`b)`
n của Mg có trong phản ứng là:
\(n_{\text{Mg}}=\dfrac{m_{\text{Mg}}}{M_{\text{Mg}}}=\dfrac{6}{24}=\dfrac{1}{4}=0,25\left(\text{mol}\right)\)
Theo PT: 1 mol Mg phản ứng với 2 mol HCl được phản ứng trên
`=> 0,25` mol Mg phản ứng với `0,5` HCl được pứ trên
Khối lượng của HCl có trong phản ứng là:
\(m_{\text{HCl}}=n_{\text{HCl}}\cdot M_{\text{HCl}}=0,5\cdot\left(1+35,5\right)=0,5\cdot36,5=18,25\left(\text{g}\right)\)
`c)`
Theo PT: 1 mol Mg phản ứng thu được 1 mol H2
`=> 0,25` mol Mg phản ứng thu được 1 mol H2
Thể tích của khí H2 thu được ở điều kiện chuẩn là:
\(\text{V}_{\text{H}_2}=\text{n}_{\text{H}_2}\cdot24,79=0,25\cdot24,79=6,1975\left(l\right)\)`.`

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, \(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}=0,4\left(mol\right)\Rightarrow m_{HCl}=0,4.36,5=14,6\left(g\right)\)
c, \(n_{H_2}=n_{Mg}=0,2\left(mol\right)\)
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
Ta có: \(n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,3}{1}>\dfrac{0,2}{1}\), ta được CuO dư.
Theo PT: \(n_{Cu}=n_{H_2}=0,2\left(mol\right)\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\\ a,PTHH:Mg+2HCl\rightarrow MgCl_2+H_2\\ n_{HCl}=2.0,2=0,4\left(mol\right);n_{H_2}=n_{Mg}=0,2\left(mol\right)\\ b,m_{HCl}=0,4.36,5=14,6\left(g\right)\\ c,n_{CuO}=\dfrac{24}{80}=0,3\left(mol\right)\\ CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\\ Vì:\dfrac{0,2}{1}< \dfrac{0,3}{1}\Rightarrow CuOdư\\ n_{Cu}=n_{H_2}=0,2\left(mol\right)\\ m_{Cu}=0,2.64=12,8\left(g\right)\)

`a)PTPƯ: Zn + 2HCl -> ZnCl_2 + H_2↑`
____________________________________________
`b) n_[Zn] = 13 / 65 = 0,2 (mol)`
Theo `PTPƯ` có: `n_[HCl] = 2n_[Zn] = 2 . 0,2 = 0,4 (mol)`
`-> m_[dd HCl] = [ 0,4 . 36,5 ] / [ 7,3 ] . 100 = 200 (g)`
_____________________________________________
`c)` Theo `PTPƯ` có: `n_[H_2] = n_[ZnCl_2] = n_[Zn] = 0,2 (mol)`
`-> C%_[ZnCl_2] = [ 0,2 . 136 ] / [ 13 + 200 - 0,2 . 2 ] . 100 ~~ 12,79 %`

a. 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
b. nH2SO4 =\(\dfrac{29,4}{98}\)=0,3 mol
Theo phương trình ta có số mol nhôm đã phản ứng là nAl= \(\dfrac{0,3.2}{3}\)= 0,1 mol ==> a = 0,1.27 = 2,7 gam
c. Phản ứng vừa đủ nên cả Al và H2SO4 cùng hết , không có chất nào dư sau phản ứng

\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Định Luật Bảo toàn khối lượng :
\(m_{Al}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2}\)
\(\Rightarrow m_{H_2}=2.7+14.7-17.1=0.3\left(g\right)\)
\(n_{H_2}=\dfrac{0.3}{2}=0.15\left(mol\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)

nFe = 2.8/56 = 0.05 (mol)
nHCl = 14.6/36.5 = 0.4 (mol)
Fe + 2HCl => FeCl2 + H2
1.........2
0.05......0.4
LTL : 0.05/1 < 0.4/2
=> HCl dư
mHCl (dư) = ( 0.4 - 0.1 ) * 36.5 = 10.95 (g)
VH2 = 0.05*22.4 = 1.12 (l)
nHCl (dư) = 0.4 - 0.1 = 0.3 (mol)
mFe cần thêm = 0.3/2 * 56 = 8.4 (g)

a) $Zn + 2HCl \to ZnCl_2 + H_2$
b) Chất phản ứng : $Zn,HCl$
Sản phẩm : $ZnCl_2,H_2$
Tỉ lệ số nguyên tử Zn : Số phân tử $HCl$ là 2 : 1
Tỉ lệ số phân tử $ZnCl_2$ : số phân tử $H_2$ là 1 : 1
c) $m_{Zn} + m_{HCl} = m_{ZnCl_2} + m_{H_2}$
d) $m_{H_2} = 26 + 29,2 - 54,4 = 0,8(gam)$
e) 1 đvC = $\dfrac{1,9926.10^{-23}}{12} = 1,6605.10^{-24}(gam)$
$m_H = 1.1,6605.10^{-24} = 1,6605.10^{-24}(gam)$
$m_{Zn} = 65.1,6605.10^{-24} = 107,9325.10^{-24}(gam)$
f)$n_{H_2} = 0,4(mol) ; n_{CO_2} = \dfrac{0,44}{44} = 0,01(mol)$
$\Rightarrow n_{hh} = 0,4 + 0,01 = 0,41(mol)$
$V_{hh} = 0,41.22,4 = 9,184(lít)$
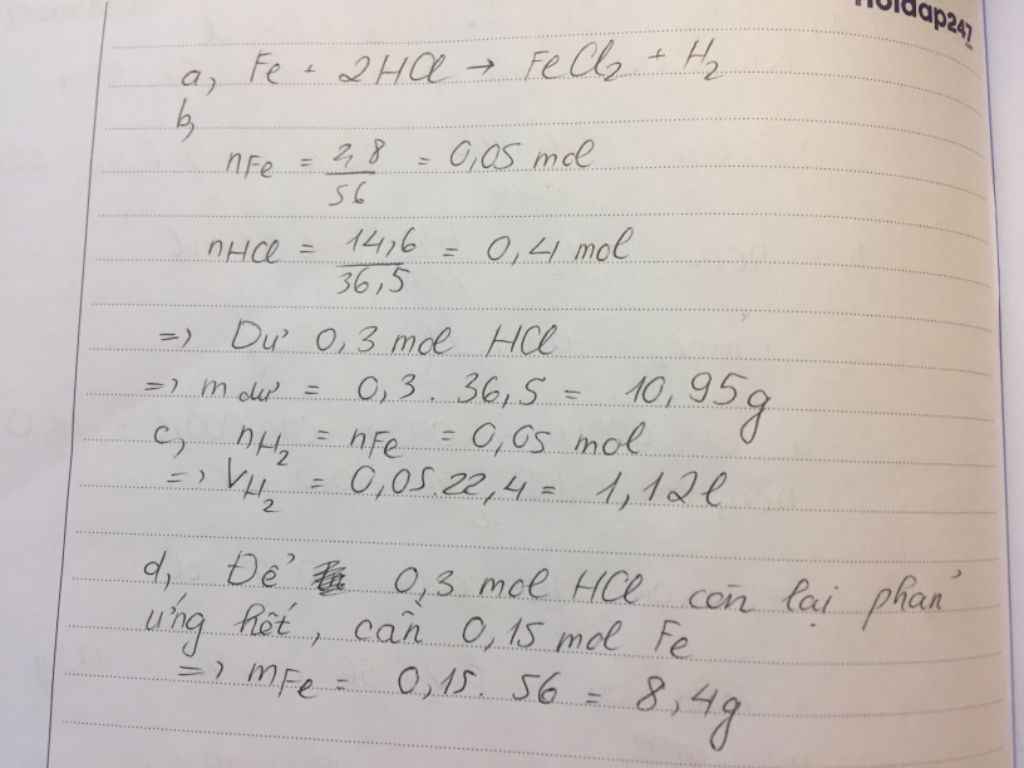
Al2O3+6HCl→2AlCl3+3H2O