Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Tính chất chung của kim loại SVIP
1. TÍNH CHẤT VẬT LÍ CỦA KIM LOẠI
Kim loại có tính dẻo, dẫn điện, dẫn nhiệt và ánh kim.
- Kim loại dễ bị biến dạng khi rèn, kéo sợi hoặc dát mỏng nhờ tính dẻo. Các kim loại có độ dẻo cao là Au, Ag, Al, Cu,...
Ví dụ: Giấy bọc thực phẩm được sản xuất từ nhôm.

- Kim loại có tính dẫn điện, các kim loại khác nhau có khả năng dẫn điện khác nhau. Dãy kim loại có tính dẫn điện theo thứ tự giảm dần là Au, Ag, Al, Cu, Sn,...
Ví dụ: Dây dẫn điện được sản xuất từ đồng (Cu).

- Kim loại có tính dẫn nhiệt. Các kim loại dẫn điện tốt thường dẫn nhiệt tốt.
Ví dụ: Nhôm được sử dụng để chế tạo xoong, nồi.

- Trên bề mặt của kim loại có vẻ sáng lấp lánh gọi là ánh kim.
Ví dụ: Vàng, bạc thường được sử dụng làm trang sức.

- Các kim loại khác nhau thường có nhiệt độ nóng chảy và khối lượng riêng khác nhau.
Câu hỏi:
@202215965879@
2. TÍNH CHẤT HÓA HỌC CƠ BẢN CỦA KIM LOẠI
➤ Phản ứng của kim loại với oxygen
Nhiều kim loại có thể phản ứng với oxygen tạo thành oxide base (trừ Au, Ag, Pt, Hg,...).
Ví dụ: Đốt cháy dây đồng trong khí oxygen.
\(2Cu+O_2\rarr2CuO\)
➤ Phản ứng của kim loại với phi kim khác
Kim loại có thể tác dụng với phi kim tạo thành muối.
Ví dụ: Bột sắt tác dụng với bột lưu huỳnh khi đun nóng.
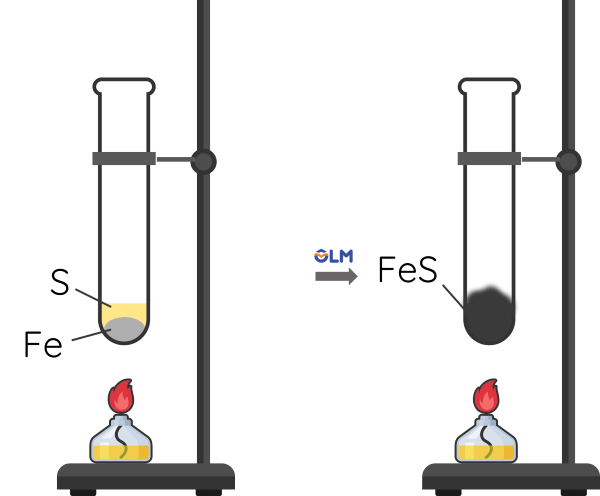
Phương trình hóa học:
\(Fe+S\overset{t^{o}}{\rarr}FeS\)
Câu hỏi:
@202866928545@
➤ Phản ứng của kim loại với nước
Các kim loại như Na, K, Ca,... phản ứng mạnh với nước tạo thành hydroxide, giải phóng khí hydrogen và tỏa nhiều nhiệt.
Ví dụ: Kim loại sodium tác dụng với nước.

Phương trình hóa học:
\(2Na+2H_2O\rarr2NaOH+H_2\)
Một số kim loại như Zn, Fe,... chỉ tác dụng với hơi nước ở nhiệt độ cao tạo thành oxide và khí hydrogen.
Ví dụ: Sắt tác dụng với hơi nước.
\(Fe+H_2O\overset{t^{o}}{\rarr}FeO+H_2\)
➤ Phản ứng của kim loại với dung dịch hydrochloric acid
Kim loại (trừ Cu, Hg, Ag, Pt, Au,...) có thể phản ứng với dung dịch hydrochloric acid tạo thành muối chloride và khí hydrogen.
Ví dụ: Magnesium phản ứng với dung dịch HCl.
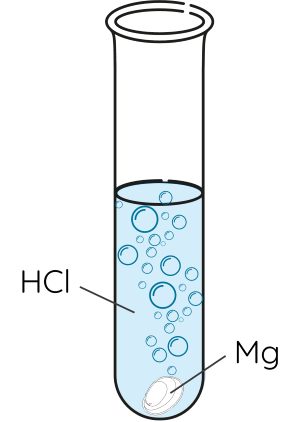
Phương trình hóa học:
\(Mg+2HCl\rarr MgCl_2+H_2\)
Câu hỏi:
@202756833431@
➤ Phản ứng của kim loại với dung dịch muối
Các kim loại (trừ K, Na, Ca,...) có thể phản ứng với dung dịch muối để tạo muối mới và kim loại mới.
Ví dụ: Sắt tác dụng với dung dịch copper(II) sulfate.
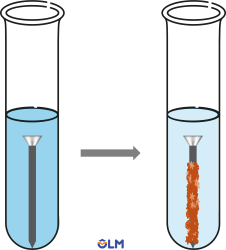
Phương trình hóa học:
\(Fe+CuSO_4\rarr FeSO_4+Cu\)
Câu hỏi:
@202756581449@
3. MỘT SỐ KHÁC BIỆT VỀ TÍNH CHẤT GIỮA CÁC KIM LOẠI THÔNG DỤNG
Nhôm, sắt và vàng có nhiều tính chất riêng biệt nên được ứng dụng rộng rãi trong đời sống và công nghiệp.
Kim loại | Nhôm | Sắt | Vàng |
|---|---|---|---|
Màu sắc | Trắng bạc | Trắng xám | Vàng |
Tính chất vật lí | Mềm, nhẹ, dẫn điện và nhiệt tốt | Cứng, dẻo, có tính nhiễm từ | Dẻo, dẫn điện và nhiệt rất tốt |
Tính chất hóa học | - Tác dụng với phi kim, dung dịch acid và dung dịch muối. - Bền trong không khí nhờ lớp oxide. | - Tác dụng với phi kim, dung dịch acid, dung dịch muối và hơi nước ở nhiệt độ cao. - Tác dụng với oxygen trong không khí. | - Không tan trong HCl, H2SO4. - Bền trong không khí. |
Ứng dụng | Dây dẫn điện, khung cửa, vách ngăn,... | Gang, thép,... | Đồ trang sức, mạch điện tử,... |
Bạn có thể đăng câu hỏi về bài học này ở đây
