Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 23 :
n BaCO3 = 0,1(mol) > n Ba(OH)2 = 0,15 mol
- TH1 : Ba(OH)2 dư
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O$
n CO2 = n BaCO3 = 0,1(mol)
=> V = 0,1.22,4 = 2,24 lít
- TH1 : BaCO3 bị hòa tan một phần
$Ba(OH)_2 + CO_2 \to BaCO_3 + H_2O(1)$
$Ba(OH)_2 + 2CO_2 \to Ba(HCO_3)_2(2)$
n CO2(1) = n Ba(OH)2 (1) = n BaCO3 = 0,1(mol)
=> n Ba(OH)2 (2) = 0,15 - 0,1 = 0,05(mol)
=> n CO2 (2) = 2n Ba(OH)2 (2) = 0,1(mol)
=> V = (0,1 + 0,1).22,4 = 4,48 lít

Ta có: \(b< a< 2b\)
`->` CO2 dư, kết tủa bị tan một phần
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
b < a ( mol )
b b b ( mol )
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
b > a-b ( mol )
a-b a-b a-b ( mol )
\(m_{CaCO_3}=100\left(b-a+b\right)=100\left(2b-a\right)\left(g\right)\)
\(m_{muối}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}\)
\(=100\left(2b-a\right)+162\left(a-b\right)\)
\(=62a+38b\left(g\right)\)

\(n_{CaCO_3} = \dfrac{30}{100} = 0,3(mol < n_{Ca(OH_2}\) nên xét 2 TH
- TH1 : Ca(OH) dư
Ca(OH)2 + CO2 → CaCO3 + H2O
....................0,3.........0,3.................(mol)
=> V = 0,3.22,4 = 6,72 lít
- TH2 : CaCO3 bị hòa tan 1 phần
Ca(OH)2 + CO2 → CaCO3 + H2O
0,5..............0,5...........0,5..................(mol)
CaCO3 + CO2 + H2O → Ca(HCO3)2
(0,5-0,3)......(0,5-0,3).............................................(mol)
=> V = (0,5 + 0,5 - 0,3).22,4 = 15,68 lít

\(a.n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ a.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\\ 0,25.......0,25............0,25..........0,25\left(mol\right)\\ C_{MddCa\left(OH\right)_2}=\dfrac{0,25}{0,1}=2,5\left(M\right)\\ b.m_{\downarrow}=m_{CaCO_3}=100.0,25=25\left(g\right)\)

Vì lượng CO2 thay đổi mà lượng kết tủa vẫn giữ nguyên nên:
Khi sục a mol CO2 thì Ca(OH)2 dư, khi sục 1,5 mol CO2 thì CaCO3 bị hoà tan một phần
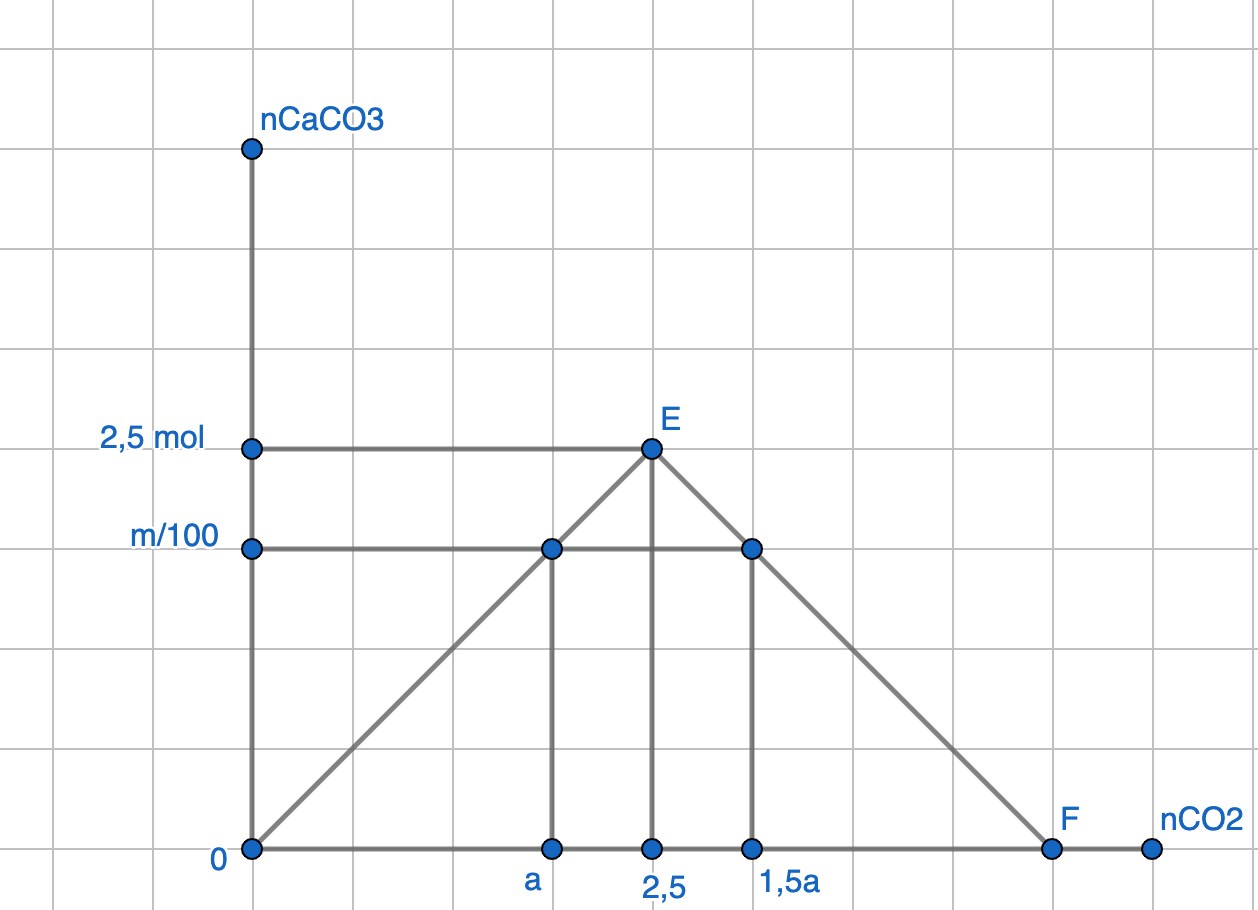
từ đồ thị suy ra: a = 2,5 .2 / 2,5 = 2 (mol)
=> m = 200g
TH1: Tạo 1 muối trung hòa
\(CO_2\left(0,03\right)+Ca\left(OH\right)_2 \left(0,03\right)\rightarrow CaCO_3\left(0,03\right)+H_2O\)
=> nCa(OH)2 phản ứng = 0,03 (mol)
TH2: Tạo muối trung hòa và muối axit
\(CO_2\left(0,03\right)+Ca\left(OH\right)_2\left(0,03\right)\rightarrow CaCO_3\left(0,03\right)+H_2O\)
\(2CO_2\left(0,02\right)+Ca\left(OH\right)_2\left(0,01\right)\rightarrow Ca\left(HCO_3\right)_2\)
=> nCa(OH)2 phản ứng = 0,04 (mol)