Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Mg+2HCl \rightarrow MgCl_2+H_2\\ Fe+2HCl \rightarrow FeCl_2+H_2\\ n_a=Mg\\ n_b=Fe\\ n_{HCl}=\frac{50.29,2\%}{36,5}=0,4mol\\ m_{hh}=24a+56b=19,2(1)\\ n_{HCl}=2a+2b=0,4(2)\\ (1)(2)\\ \)
Xem lại đè bài nha

mHCl=29,2%. 50=14,6(g)
=>nHCl=14,6/36,5= 0,4(mol)
Đặt : nNaOH=a(mol); nCa(OH)2=b(mol) (a,b>0)
PTHH: NaOH + HCl -> NaCl + H2O
a_____________a____a(mol)
Ca(OH)2 + 2 HCl -> CaCl2 + 2 H2O
b______2b_______b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}40a+74b=15,4\\a+2b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
\(\%mNaOH=\dfrac{0,2.40}{15,4}.100\approx51,95\%\)
=> CHỌN B

Gọi số mol của Zn, Mg và Fe lần lượt là x, y và z mol
TN1: tác dụng với dung dịch HCl tạo 0,5 mol khí H2
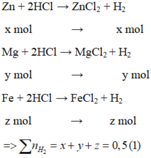
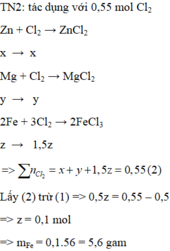
Đáp án: B

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Gọi: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\) ⇒ 24x + 56y = 8 (1)
Theo PT: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=x\left(mol\right)\\n_{FeCl_2}=n_{Fe}=y\left(mol\right)\end{matrix}\right.\) ⇒ 95x + 127y = 22,2 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,1.24}{8}.100\%=30\%\\\%m_{Fe}=70\%\end{matrix}\right.\)
b, \(n_{HCl}=2n_{Mg}+2n_{Fe}=0,4\left(mol\right)\)
\(\Rightarrow V_{ddHCl}=\dfrac{0,4}{1}=0,4\left(l\right)\)

Fe +2HCl---.--->FeCl2 +H2
x-----------------------x
Mg+2HCl----->MgCl2+H2
y------------------y
Ta có
m\(_{Fe}=56x\)
m\(_{Mg}=24y\)
m\(_{FeCl2}=127x\)
m\(_{MgCl2}=95y\)
Theo bài ra ta có hệ pt
\(\left\{{}\begin{matrix}56x+24y=8\\127x+95y=22,2\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
%m\(_{Fe}=\frac{0,1.56}{8}.100\%=70\%\%=\)
%m\(_{Mg}=100-70=30\%\)

Gọi nFe =x, nMg= y, m đdHCl=m
Theo m hhX= 56x + 24y=13,3
Fe + 2H+ -> H2 + Fe2+ và Mg + 2H+ -> H2 + Mg2+
x------> 2x ---> x y -----> 2y---> y
Nông đọ của HCl = (nH+ . M HCl) / mddHCl = 2. 36,5 . (x+y)/m=0,1591
<=> 72x + 72 y -0,1591m=0
Nồng đọ của muối sắt= 127x/ (m + 13,3- 2x- 2y)=0,1523
<=> 127,3046x + 0,3046y - 0,1523m= 2,02559
Giải 3 phương trình trên ta có được x≈ 0,18 y≈ 0,126 m ≈140,178
=> %m Fe= 0,18 . 56. 100/13,3 ≈ 77,183 % % mMg = 22, 817 %
% MgCl2 = 0,126. 95. 100 / (140, 178 + 13,3 - 2.(0.18 + 0, 126))≈ 7,86%
Theo mình nghĩ baig này giải như thế này:
Gọi nFe =x, nMg= y, m đdHCl=m
Theo m hhX= 56x + 24y=13,3
Fe + 2H+ -> H2 + Fe2+ và Mg + 2H+ -> H2 + Mg2+
x------> 2x ---> x y -----> 2y---> y
Nông đọ của HCl = (nH+ . M HCl) / mddHCl = 2. 36,5 . (x+y)/m=0,1591
<=> 72x + 72 y -0,1591m=0
Nồng đọ của muối sắt= 127x/ (m + 13,3- 2x- 2y)=0,1523
<=> 127,3046x + 0,3046y - 0,1523m= 2,02559
Giải 3 phương trình trên ta có được x≈ 0,18 y≈ 0,126 m ≈140,178
=> %m Fe= 0,18 . 56. 100/13,3 ≈ 77,183 % % mMg = 22, 817 %
% MgCl2 = 0,126. 95. 100 / (140, 178 + 13,3 - 2.(0.18 + 0, 126))≈ 7,86%

a, Ta có: 27nAl + 56nFe = 22 (1)
PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Fe}=\dfrac{19,832}{24,79}=0,8\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,4\left(mol\right)\\n_{Fe}=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,4.27}{22}.100\%\approx49,09\%\\\%m_{Fe}\approx50,91\%\end{matrix}\right.\)
b, \(n_{HCl}=2n_{H_2}=1,6\left(mol\right)\)
\(\Rightarrow C_{M_{HCl}}=\dfrac{1,6}{0,5}=3,2\left(M\right)\)
Fe + 2HCl ----> FeCl2 + H2
Mg + 2HCl ----> MgCl2 + H2
Gọi x là số mol Fe, y là số mol Mg
\(\left\{{}\begin{matrix}56x+24y=19,2\\2x+2y=\dfrac{50.29,2\%}{36,5}=0,4\left(mol\right)\end{matrix}\right.\)
=> x=0,45; y=-0,25
Xem lại đề !
A