
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Hai phương pháp điều chế H2S từ những chất trên.
Fe + S -> FeS (1)
FeS + H2SO4 -> FeSO4 + H2S (2)
Fe + H2SO4 -> FeSO4 + H2 (3)
H2 + S -> H2S (4)
b) Vai trò của S trong phản ứng (1), (4) : S là chất oxi hóa.
Đỗ Hương Giang21 tháng 4 2017 lúc 19:40
a) Hai phương pháp điều chế H2S từ những chất trên.
Fe + S -> FeS (1)
FeS + H2SO4 -> FeSO4 + H2S (2)
Fe + H2SO4 -> FeSO4 + H2 (3)
H2 + S -> H2S (4)
b) Vai trò của S trong phản ứng (1), (4) : S là chất oxi hóa.

a)
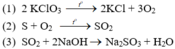
Phản ứng oxi hóa – khử là (1) và (2).
b)
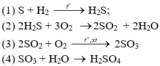
Phản ứng oxi hóa – khử là: (1), (2), (3)

\(S+H_2\underrightarrow{t^o}H_2S\)
\(2H_2S+3O_2\underrightarrow{t^o}2SO_2+2H_2O\)
\(2SO_2+O_2\underrightarrow{t^o}2SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)

Câu1:
- Trích mẫu thử
- Cho quỳ tìm vào các mẫu thử
+ mẫu thử nào làm quỳ tím hóa đỏ là HCl
+ mẫu thử nào làm quỳ tím hóa xanh là NaOH
+ các mẫu thử còn lại không hiện tượng là NaCl,NaNO3,NaBr
- Cho dd \(AgNO_3\) tới dư vào các mẫu thử còn lại :
+ mẫu thử nào tạo kết tủa trắng là NaCl
NaCl+\(AgNO_3\) →AgCl↓+ \(NaNO_3\)
+ mẫu thử nào tạo kết tủa màu vàng nhạt là NaBr
NaBr+ \(AgNO_3\) →AgBr↓+ \(NaNO_3\)
+ mẫu thử nào không có hiện tượng là \(NaNO_3\)
Câu 2:
1. \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2\uparrow+8H_2O\)
2. \(Cl_2+2Na\underrightarrow{t^o}2NaCl\)
3. \(2NaCl\underrightarrow{đpnc}2Na+Cl_2\)
4.\(2HBr+Cl_2\rightarrow2HCl+Br_2\)
\(2NaI_{\left(lạnh\right)}+Br_2\rightarrow2NaBr+I_2\)
Câu 3 :
\(a) n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b =1 1,1(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{6,72}{22,4} = 0,3(2)\\ (1)(2) \Rightarrow a = 0,1 ; b = 0,15\\ \%m_{Al} = \dfrac{0,1.27}{11,1}.100\% = 24,32\%\\ \%m_{Fe} = 100\% -24,32\% = 75,68\%\)
\(b) n_{HCl} = 2n_{H_2} = 0,3.2 = 0,6(mol)\\ \Rightarrow m_{dd\ HCl} = \dfrac{0,6.36,5}{14,6\%} = 150(gam)\\ m_{dd\ sau\ pư} = m_{hỗn\ hợp} + m_{dd\ HCl} - m_{H_2} = 11,1 + 150 - 0,3.2 = 160,5(gam)\\ n_{AlCl_3} = a = 0,1(mol)\ ;\ n_{FeCl_2} = b = 0,15(mol)\\ C\%_{AlCl_3} = \dfrac{0,1.133,5}{160,5}.100\% =8,32\%\\ C\%_{FeCl_2} = \dfrac{0,15.127}{160,5}.100\% = 11,87\%\)
