Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Axit formic là axit yếu. Tuy nhiên nó mạnh nhất trong dãy đồng đẳng của axit cacboxylic no, đơn chức, mạch hở và mạnh hơn axit cacbonic:(H2CO3) do hiệu ứng dồn mật độ electron trong nhóm
-COOH. Axit cacboxylic không có phản ứng tráng bạc nhưng riêng HCOOH thì có.
Phương trình phản ứng như sau:
HCOOH + 2[Ag(NH3)2]OH → (NH4)2CO3 + 2Ag↓ + 2NH3↑ + H2O

Có thể thực hiện như sau:
Cho hai giọt dung dịch phenolphtalein vào dung dịch Ca(OH)2 ta thu được dung dịch A có màu hồng.
Dẫn ba chất khí đó lần lượt vào ba ống nghiệm riêng biệt.
Nhỏ vài giọt dung dịch A vào trong ba ống nghiệm đựng CO, HCl, SO2
Nếu có kết tủa trắng và dung dịch mất màu, đó là ống nghiệm đựng SO2.
Nếu dung dịch A mất màu, đó là ống nghiệm đựng HCl.
Nếu màu dung dịch không thay đổi, đó là ống nghiệm đựng CO.
Ngoài ra có thể sử dụng các thuốc thử khác vẫn có thể nhận biết được từng lọ đựng khí.

Khí CO2 phản ứng với nước vôi trong, hơi nước bị giữ lại khi qua CaCl2 khan, còn CO thì không. Do đó, hỗn hợp khí qua nước vôi trong rồi qua bình đựng CaCl2 khan thì thu được CO. Ngoài ra, có thể dùng hóa chất khác nếu CO không có phản ứng với chất đó và chất đó giữ lại CO2, hơi nước.

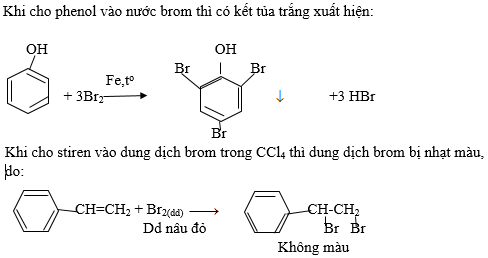
- Dung dịch bị vẩn đục là do phản ứng tạo ra phenol.
- Nhận xét về tính axit của phenol: Phenol có tính axit yếu hơn nấc thứ nhất của axit cacbonic H2CO3, nên bị axit cacbonic đẩy ra khỏi dung dịch muối.

a) C2H4 + O2 -> CH3CHO
Hỗn hợp khí X gồm C2H4 chưa phản ứng và CH3CHO. Khi X tác dụng với dung dịch AgNO3/NH3
CH3CHO + 2AgNO3 + 3NH3 + H2O -> CH3COONH4 + 2Ag + 2NH4NO3
Số mol Ag = 0,150 mol. Vậy số mol CH3CHO = 0,0750 mol
Hiệu suất của quá trình oxi hóa etilen :  .100% = 75%
.100% = 75%

Hướng dẫn.
CnH2n+2 +3n+123n+12O2 to→→to nCO2 + (n+1)H2O có nCO2nH2OnCO2nH2O < 1.
CnH2n + 3n23n2O2 to→→to nCO2 + nH2O có nCO2nH2OnCO2nH2O = 1.
CnH2n-2 + 3n−123n−12O2 to→→to nCO2 + (n-1)H2O có nCO2nH2OnCO2nH2O > 1.
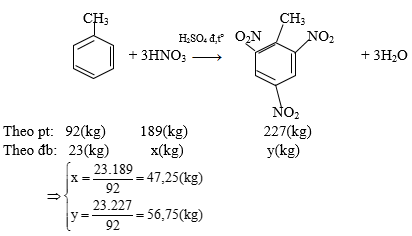
CnH2n-6 + 3n−323n−32O2 to→→to nCO2 + (n-3)H2O có nCO2nH2OnCO2nH2O > 1.
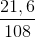 = 0,2 (mol)
= 0,2 (mol)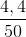 . 100% = 8,8%
. 100% = 8,8%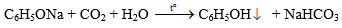
3. Viết phương trình hóa học của các phản ứng hoàn thành dãy chuyển hóa sau:
a) Etan (1)→→(1) etilen (2)→→(2) politilen.
b) Metan (1)→→(1) axetilen (2)→→(2) vinylaxetilen (3)→→(3) butanđien (4)→→(4) polibutađien.
c) Benzen → brombenzen.
Hướng dẫn.
a) (1) C2H6 to,xt→→to,xt C2H4 + H2
(2) nCH2 = CH2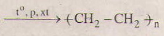
b) (1) 2CH4 1500oC→→1500oC C2H2 + 3H2
(2) 2CH ≡ CH to,xt→→to,xt CH2 = CH – C ≡ CH
(3) CH2 = CH – C ≡ CH + H2 Pd/PbCO3−−−−−−→to→toPd/PbCO3 CH2 = CH – CH = CH2
(4) nCH2 = CH – CH – CH2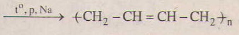
c)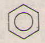 + Br Fe−→to→toFe
+ Br Fe−→to→toFe 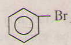 + HBr
+ HBr