Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nbbnbnv ghvghgggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggggg

1.
Ta có: \(\left\{{}\begin{matrix}p+e+n=52\\p=e\\n=1,06e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)
2.
Ta có: \(\left\{{}\begin{matrix}p+e+n=49\\p=e\\n=53,125\%\left(p+e\right)\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=16\\n=17\end{matrix}\right.\)
Ý 1:
\(\left\{{}\begin{matrix}P+N+E=52\\N=1,06E\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2E+N=52\\N=1,06E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}E=P=Z=17\\N=18\end{matrix}\right.\\ \Rightarrow A=17+18=35\left(đ.v.C\right)\\ KH.nguyên.tử:^{35}_{17}Cl\)
Ý 2:
\(\left\{{}\begin{matrix}P+N+E=49\\N=53,125\%\left(P+E\right)\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=49\\N-1,0625P=0\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}N=17\\P=E=Z=16\end{matrix}\right.\Rightarrow A=17+16=33\left(đ.v.C\right)\\ kí.hiệu.nguyên.tử:^{33}_{16}S\)

Câu hỏi tương tự: Câu hỏi của N.H. Dũng - Hóa học lớp 10 | Học trực tuyến

-Bài 1:Ta có P=E
2P+N=40
N-P=1
Giải hệ có P=E=13(Al) và N=14
-Bài 2:Ta có P=E
2P+N=52
N=1,06E
Giải hệ có P=E=17(Cl) và N=18
Bài 1:
Ta có: 2P+N=40
N-P=1
Giải hệ phương trình ta được P=13 (Al)

Chọn D
Theo bài ra ta có hệ phương trình:
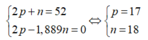
Cấu hình electron của X là [ N e ] 3 s 2 3 p 5 → X có 7e lớp ngoài cùng nên là phi kim.
Số khối của X là: 18 + 17 = 35.
Điện tích hạt nhân X là 17+.

a) Ta có: p+e+n=82
Mà p=e \(\rightarrow\) 2p+n=82 (1)
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 22 hạt
\(\rightarrow\) 2p-n=22 (2)
Từ (1) và (2)\(\rightarrow\) p=26, n=30
\(\rightarrow\)Nguyên tố đó là Sắt (Fe)
b) Ta có: 2p+n=52 (2)
n=1,058e (1)
Vì p=e \(\rightarrow\)(1) ⇔ n=1,058p\(\rightarrow\) -1,058p+n=0 (3)
Từ (2) và (3) \(\rightarrow\) p=17, n=18
Vậy nguyên tố đó là Clo (Cl)
c) Ta có: 2p+n=58\(\rightarrow\)n=58-2p (1)
Ta có hệ thức: \(\text{p≤n≤1,5p (2)}\)
Thế (1) vào (2)\(\rightarrow\)\(\text{ p≤58-2p≤1,5p}\)
\(\text{⇔ 3p≤58≤3,5p}\)
\(\text{⇔ 16,57 ≤ p≤19,33 }\)
\(\rightarrow\) p có thể bằng 17,18,19
Nếu p=17\(\rightarrow\)n=24\(\rightarrow\) Số khối A= p+n= 17+24= 41 (>40 \(\Rightarrow\) Loại)
Nếu p=18 \(\rightarrow\) n=22\(\rightarrow\) A= 40 (Loại vì theo đề thì A <40)
Nếu p=19 ==> n= 20 ==> A=39 (Là nguyên tố K)
Vậy nguyên tố đó là Kali (K)
Giải:
Theo đề ra, ta có:
\(p+e+n=52\)
\(n=1,06p\)
Mà p = e
Ta có hpt:
\(\left\{{}\begin{matrix}2p+n=52\\1,06p-n=0\end{matrix}\right.\)
Giải hpt, được:
\(\left\{{}\begin{matrix}p=e=17\\n=18\end{matrix}\right.\)
Vậy ...