Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
1 1 1 1
0,3 0,3 0,3 0,3
\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
a). \(n_{H2}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒\(V_{H2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b). \(80ml=0,08l\)
\(n_{H2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
→\(C_M=\dfrac{n}{V}=\dfrac{0,3}{0,08}=3,75\left(M\right)\)
c). \(n_{MgSO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(V_{MgSO4}=n.22,4=0,3.22,4=6,72\left(l\right)\)
→\(C_M=\dfrac{n}{V}=\dfrac{0,3}{6,72}=0,04\left(M\right)\)
d). \(MgSO_4+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2+BaSO_4\downarrow\)
1 1 1 1
0,3 0,3 0,3
\(n_{BaSO4\uparrow}=\dfrac{0,3.1}{1}\)=0,3(mol)
→\(m_{BaSO4\downarrow}=n.M=0,3.233=69,9\left(g\right)\)
\(n_{Ba\left(OH\right)_2}=\dfrac{0,3.1}{1}\)=0,3(mol)
\(\rightarrow V_{ddBa\left(OH\right)_2}=\dfrac{n}{C_M}=\dfrac{0,3}{1,6}=0,1875\left(l\right)\)

\(n_{Na2CO3}=\dfrac{10,6}{106}=0,1\left(mol\right)\)
\(2CH_3COOH+Na_2CO_3\rightarrow2CH3OONa+CO_2+H_2O\)
0,2 0,1 0,2 0,1
a) \(V_{CO2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
\(C_{MCH3COOH}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
b) \(C_{MCH3COONa}=\dfrac{0,2}{0,2}=1\left(M\right)\)
Chúc bạn học tốt

a, \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\right)\)
\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
PT: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
Xét tỉ lệ: \(\dfrac{0,15}{1}< \dfrac{0,4}{2}\), ta được HCl dư.
Theo PT: \(n_{H_2}=n_{Fe}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)=3360\left(ml\right)\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{Fe}=0,15\left(mol\right)\\n_{HCl\left(pư\right)}=2n_{Fe}=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{HCl\left(dư\right)}=0,4-0,3=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{FeCl_2}}=\dfrac{0,15}{0,2}=0,75\left(M\right)\\C_{M_{HCl\left(dư\right)}}=\dfrac{0,1}{0,2}=0,5\left(M\right)\end{matrix}\right.\)
c, Ta có: \(m_{ddHCl}=1,25.200=250\left(g\right)\)
⇒ m dd sau pư = 8,4 + 250 - 0,15.2 = 258,1 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,15.127}{258,1}.100\%\approx7,38\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,1.36,5}{258.1}.100\%\approx1,41\%\end{matrix}\right.\)

\(n_{Na_2CO_3}=\dfrac{360.21,2\%}{100\%.106}=0,72(mol)\\ n_{H_2SO_4}=2,5.0,2=0,5(mol)\\ PTHH:Na_2CO_3+H_2SO_4\to Na_2SO_4+H_2O+CO_2\uparrow\\ a,\text {Vì }\dfrac{n_{Na_2CO_3}}{1}>\dfrac{n_{H_2SO_4}}{1} \text {nên }Na_2CO_3\text { dư}\\ \Rightarrow n_{CO_2}=n_{H_2SO_4}=0,5(mol)\\ \Rightarrow V_{CO_2}=0,5.22,4=11,2(l)\\\)
\(b,A:Na_2SO_4\\ n_{Na_2SO_4}=n_{H_2SO_4}=0,5(mol)\\ m_{dd_{H_2SO_4}}=200.1,1=220(g);V_{dd_{Na_2CO_3}}=\dfrac{360}{1,2}=300(ml)=0,3(l)\\ \Rightarrow C\%_{Na_2SO_4}=\dfrac{0,5.142}{360+200-0,5.44}.100\%=13,2\%\\ C_{M_{Na_2SO_4}}=\dfrac{0,5}{0,3+0,2}=1M\)

\(a.Zn+H_2SO_4\rightarrow ZnSO_4+H_2\\ n_{Zn}=\dfrac{4,55}{65}=0,07\left(mol\right)\\ n_{H_2}=n_{Zn}=0,07\left(mol\right)\\ \Rightarrow V_{H_2}=0,07.22,4=1,568\left(l\right)\\ b.n_{HCl}=2n_{Zn}=0,14\left(mol\right)\\ \Rightarrow CM_{HCl}=\dfrac{0,14}{0,2}=0,7M\\ c.n_{ZnCl_2}=n_{Zn}=0,07\left(mol\right)\\ \Rightarrow m_{ZnCl_2}=0,07.136=9,52\left(g\right)\)

m dd A = 4 . 79,3 = 317,2g
Qui đổi hỗn hợp FeO, Fe2O3, Fe3O4về Fe3O4 có số mol là a
Ta có 232a + (a . 4 . 1,5 . 98) : 0,2 = 317,2
=> a = 0,1 mol
Dd ban đầu
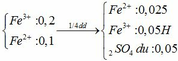
Phần 1:
8H2SO4 + 2KMnO4 + 10FeSO4 → 5Fe2(SO4)3 + 8H2O + 2MnSO4 + K2SO4
0,05 0,025
=> FeSO4 phản ứng hết
=> nKMnO4 = 0,005mol
=> V1= 0,1 lít = 100ml
Phần 2:
2Fe2+ + Br2 → 2Fe3+ + 2Br-
0,025 0,0125
=> V2 = 0,25 lít = 250ml
Phần 3:
2Fe3+ + 2I- → 2Fe2+ + I2
0,05 0,05
=> V3 = 1 lít = 1000ml
Phần 4:
Fe2+ + CO32- → FeCO3↓
0,025 0,025 0,025
2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3 + 3CO2
0,05 0,075 0,05 0,075
2H+ + CO32- →CO2 + H2O
0,1 0,05 0,05
=> nCO2 = 0,125
=> V4 = 2,8 lít
m kết tủa = mFeCO3 + mFe(OH)3 = 8,25g