Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. 1 mol chất có chưa NA phân tử, n mol chất có N phân tử
Do đó: N = n . N A = m μ H 2 O . N A = 200 18 .6 , 02.10 23 ≈ 6 , 68.10 24 phân tử
b. Số phân tử chứa trong 1kg không khí
N = 22 % . m μ O 2 N A + 78 % m μ N 2 N A = m . N A . [ 22 % 32 + 78 % 28 ] ≈ 2 , 1.10 25 phân tử

a. 1 mol chất có chưa NA phân tử, n mol chất có N phân tử
Do đó: N = n . N A = m μ H 2 O . N A = 200 18 .6 , 02.10 23 ≈ 6 , 68.10 24 phân tử
b. Số phân tử chứa trong 1kg không khí
N = 22 % . m μ O 2 N A + 78 % m μ N 2 N A = m . N A . [ 22 % 32 + 78 % 28 ] ≈ 2 , 1.10 25 phân tử

Khối lượng ôxi trong 1,2kg không khí:
m O 2 = 1200.22 100 = 264 g a m .
Khối lượng nitơ trong 1,2kg không khí:
m N 2 = 1200.78 100 = 936 g a m .
Số phân tử ôxi:
N = 264 32 .6 , 02.10 23 = 49 , 66.10 23 phân tử.
Số phân tử nitơ:
N ' = 936 28 .6 , 02.10 23 = 201 , 24.10 23 phân tử.
Suy ra số phân tử trong 1,2kg không khí:
N 0 = N + N ' = 250 , 9.10 25 phân tử.

Gọi bán kính của hình cầu là R thì dung tích của bình là
\(V=\frac{4}{3}\pi R^3=1l=10^{-3}m^3\). Suy ra : \(R\approx0,06\)
Diện tích mặt cầu là \(S=4\pi R^2\). Một phân tử khí chiếm diện tích là \(d^2=10^{-20}m^2\)
Số đơn phân tử bám vào thành bình là \(N=\frac{4\pi R^2}{d^2}\). Ở nhiệt độ \(300^oC\), số phân tử ở thành bình sẽ được giải phóng và chiếm toàn bộ dung tích của bình. Vậy mật độ phân tử khí trong bình là :
\(n=\frac{N}{V}=\frac{3}{d^2R}=5.10^{21}m^{-3}\)

Khi không khí chưa thoát ra khỏi phòng:
p 0 V 0 = m 0 μ R T ⇒ m 0 = p 0 V 0 μ R T 0 (1)
Khi không khí đã thoát ra khỏi phòng thì với lượng không khí còn lại trong phòng:
p 1 V 1 = m 1 μ R T ⇒ m 1 = p 1 V 1 μ R T 1 = p 1 V 0 μ R T 1 (2)
Từ (1) và (2)
⇒ m 1 = m 0 T 1 p 2 T 2 p 1 = ρ 0 V 0 T 0 p 1 T 1 p 0 ⇒ m 1 = 1 , 293.4.5.8 273.78 283.76 m 1 = 204 , 82 ( k g )
Thể tích khí thoát ra ở điều kiện chuẩn là:
Δ V 0 = Δ m ρ 0 = m 0 − m 1 ρ 0 ∆ V o = 206 , 88 − 204 , 82 1 , 293 = 1 , 59 m 3

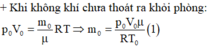
+ Khi không khí đà thoát ra khỏi phòng thì với lượng không khí còn lại trong phòng:


1.ta có V^2-Vo^2=2as ( vs a=-g vì cđ ném lên) =>s=(-100)/-20=5m
2. viết pt2niuton .chọn chiều hướng nên là chiều+ :<=>P+Fc=ma(pt vecto)
chiếu + =>-p-f=ma <=>-1.05g=a =>a=-10.5
ta có V^2-Vo^2=2as =>s =-Vo^2/2a =>s=4.7619m
vật cđ xuống =>pt2niuron:P+Fc=ma ( chọn chiều + là chiều hướng xuống)
chiếu +:p-f=ma<=>0.95g=a =>a=9.5
V^2-Vo^2=2as =>V=\(\sqrt{2as}\) =>V=9.51

Số mol khí: n = N/ N A (N là số phân tử khí)
Mặt khác n = m/ μ . Do đó: μ = m N A /N = 15.6,02. 10 23 /5,46. 10 26 = 16,01. 10 - 3 (kg/mol) (1)
Trong các khí có hidro và cacbon thì C H 4 có:
μ = (12 + 4). 10 - 3 kg/mol (2)
So sánh (2) với (1) ta thấy phù hợp. Vậy khí đã cho là C H 4
Khối lượng của phân tử hợp chất là: m C H 4 = m/N
Khối lượng của nguyên tử hidro là:
m H 4 = 4/16 . m C H 4 = 4/16 . m/N ≈ 6,64. 10 - 27 (kg)
Khối lượng nguyên tử cacbon là:
m C = 12/16 . m C H 4 = 12/16 . m/N ≈ = 2. 10 - 26 (kg)

Ta có ρ = 13 , 6 ( k g / d m 3 ) = 13 , 6 ( g / c m 3 )
Trạng thái 1 { V 1 = 14 ( c m 3 ) T 1 = 77 + 273 = 350 K Trạng thái 2 { V 2 T 2 = 273 + 27 = 300 K
Áp dụng định luật Gay – Luyxắc
V 1 V 2 = T 1 T 2 ⇒ V 2 = V 1 . T 2 T 1 = 14. 300 350 V 2 = 12 ( c m 2 )
Vậy lượng thể tích đã chảy vào bình là Δ V = V 1 − V 2 = 14 − 12 = 2 ( c m 3 )
Khối lượng thủy ngân chảy vào bình m = ρ . Δ V = 13 , 6.2 = 27 , 2 ( g )
Số phân tố chứa trong lkg không khí: