Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

| Số mol | Số phân tử |
| \(n_{SO_3}=\dfrac{16}{80}=0,2\left(mol\right)\) | \(0,2.6.10^{23}=1,2.10^{23}\left(p.tử\right)\) |
| \(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\) | \(0,2.6.10^{23}=1,2.10^{23}\left(p.tử\right)\) |
| \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{16}{400}=0,04\left(mol\right)\) | \(0,04.6.10^{23}=2,4.10^{22}\left(p.tử\right)\) |
| \(n_{Al_2\left(SO_4\right)_3}=\dfrac{34,2}{342}=0,1\left(mol\right)\) | \(0,1.6.10^{23}=6.10^{22}\left(p.tử\right)\) |
a) \(n_{SO3}=\dfrac{16}{80}=0,2\left(mol\right)\)
⇒ \(A=0,2.6.10^{-23}=1,2.10^{-23}\) (phân tử)
b) \(n_{NaOH}=\dfrac{8}{40}=0,2\left(mol\right)\)
⇒ \(A=0,2.6.10^{-23}=1,2.10^{-23}\) (phân tử)
c) \(n_{Fe2\left(SO4\right)3}=\dfrac{16}{400}=0,04\left(mol\right)\)
⇒ \(A=0,04.6.10^{-23}=0,24.10^{-23}\) (phân tử)
d) \(n_{Al2\left(SO4\right)3}=\dfrac{34,2}{342}=0,1\left(mol\right)\)
⇒ \(A=0,1.6.10^{-23}=0,6.10^{-23}\) (phân tử)
Chúc bạn học tốt

Ta có: \(n_{CO_2}=\dfrac{4,4}{44}=0,1\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{3,6}{18}0,2\left(mol\right)\Rightarrow n_H=0,2.2=0,4\left(mol\right)\)
⇒ mC + mH = 0,1.12 + 0,4.1 = 1,6 (g) < mA
→ A gồm C, H và O.
⇒ mO = 3,2 - 1,6 = 1,6 (g)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Gọi CTPT của A là CxHyOz.
⇒ x:y:z = 0,1:0,4:0,1 = 1:4:1
→ CTPT của A có dạng là (CH4O)n
\(\Rightarrow n=\dfrac{32}{12+1.4+16}=1\)
Vậy: CTPT của A là CH4O.
b, CTCT: CH3OH.
PT: \(CH_3OH+Na\rightarrow CH_3ONa+\dfrac{1}{2}H_2\)

a) Gọi x là số mol CuO => 2x là số mol ZnO
Ta có : 80x + 81.2x =12,1
=> x=0,05
=> \(\%m_{CuO}=\dfrac{0,05.80}{12,1}.100=33,06\%\);\(\%m_{ZnO}=66,94\%\)
b)CuO + 2HCl --------> CuCl2 + H2O
ZnO + 2HCl --------> ZnCl2 + H2O
\(CM_{HCl}=\dfrac{0,05.2+0,1.2}{0,1}=3M\)

CTPT hiđrocacbon là CxHy ( x, y ∈ N và 0< y ≤ 2x + 2)
CxHy + (x + 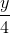 ) O2 → x CO2 +
) O2 → x CO2 + 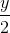 H2O
H2O
0,1 mol → 0,1x→ 0,05y
=> Khối lượng CO2 + Khối lượng H2O = 0,1.x . 44 + 0,05y. 18 =23
=> y = 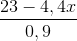
=> 0 < 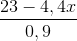 ≤ 2x + 2
≤ 2x + 2
=> 3,3 < x < 5,2 => x = 4 hoặc x =5
Nếu x = 4 => y =6 => CTPT là C4H6. Nếu x =5 => y = 1,1 ( Loại)
Vậy công thức phân tử của hiđrocacbon thỏa mãn là C4H6.
Công thức cấu tạo mạch hở có thể có:
CH2 = CH – CH = CH2
CH2 = C= CH – CH3
CH ≡ C – CH2 – CH3
CH3 – C ≡ C – CH3

Axit H3PO4 là axit 3 nấc nên phản ứng với NaOH có thể xảy ra 3 phương trình như sau
H3PO4 +3NaOH =>Na3PO4 +3H2O
H3PO4 +2NaOH =>Na2HPO4 +2H2O
H3PO4+NaOH =>NaH2PO4 +H2O
Xét tỉ lệ mol NaOH/mol H3PO4=T
Nếu T=1=>chỉ tạo muối NaH2PO4 Tương tự với T=2;T=3
ở đây đbài của bạn là 0,625/0,4=1,5625 T nằm giữa khoảng 1 và 2 nên sẽ ra 2 muối NaH2PO4 và Na2HPO4
Pt đó không sai nhưng nếu bạn chưa học về dung dịch điện li thì hãy viết 2NaOH+H3PO4 đặt ẩn giải hpt cho đỡ rối

Câu 1: Nếu 2 chất khí khác nhau nhưng đo ở cùng nhiệt độ và áp suất thì chúng có
A. Cùng khối lượng B. Cùng số mol
C. Cùng tính chất hóa học D. Cùng tính chất vật lí
Câu 2: Tính số nguyên tử của 1,8 mol Fe
A. 10,85.10 23 nguyên tử B. 10,8.10 23 nguyên tử
C. 11.10 23 nguyên tử D. 1,8.10 23 nguyên tử
Câu 3: Khối lượng mol chất là
A. Là khối lượng ban đầu của chất đó
B. Là khối lượng sau khi tham gia phản ứng hóa học
C. Bằng 6.10 23
D. Là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó
Câu 4: Cho biết 1 mol chất khí ở điều kiện bình thường có thể tích là
A. 2,24 l B. 0,224 l C. 24 l D. 22,4 ml
P/s: Điều kiện 20 độ C, áp suất 1 atm
Câu 5: Tính thể tích ở đktc của 2,25 mol O 2
A. 22,4 l B. 24 l C. 5,04 l D. 50,4 l
Câu 6: Số mol của H 2 ở đktc biết V= 5,6 l
A. 0,25 mol B. 0,3 mol C. 0,224 mol D. 0,52 l
Câu 7: Thể tích mol là
A. Là thể tích của chất lỏng B. Thể tích của 1 nguyên tử nào đó
C. Thể tích chiếm bởi N phân tử của chất khí đó D. Thể tích ở đktc là 22,4 l
Câu 8: Số mol của kali 1,5.10 23 nguyên tử kali là
A. 1 mol B. 1,5 mol C. 0,5 mol D. 0,25 mol
Câu 9: Chọn đáp án sai:
A. Khối lượng của N phân tử CO 2 là 18 g B. M H2 O = 18 g/mol
C. 1 mol O 2 ở đktc là 24 l D.Thể tích mol của chất khí phải cùng t 0 và áp suất
P/s: M= 44 g/mol
Câu 10: Ở đktc 8 mol N 2 cố thể tích là
A. 179,2 l B. 17,92 l C. 0,1792 l D. 1,792 l
Câu 11: Cho 2,3 g Na phản ứng hết với oxi, sau phản ứng thu được natri oxit.khối
lượng chất tạo thành la
A. 0,31 g B. 3 g C. 3,01 g D. 3,1 g
Câu 12: Cho sơ đồ phản ứng sau Fe + H 2 SO 4 → FeSO 4 + H 2 , biết m Fe = 15,12 g Thể
tích hiđro thu được là
A. 6,048 l B. 8,604 l C. 5,122 l D. 2,45 l
Câu 13: Số mol của 12g O 2 , 1,2 g H 2 , 14 g N 2 lần lượt là
A. 0,375 mol; 0,6 mol; 0,5 mol B. 0,375 mol; 0,5 mol; 0,1 mol
C. 0,1 mol; 0,6 mol; 0,5 mol D. O,5 mol; 0,375 mol; 0,3 mol
Câu 14: Ở đktc 96 (g) CH 4 có thể tích là
A. 134,4 ml B. 0,1344 ml C. 13,44 ml D. 1,344 ml
Câu 15: Số mol nguyên tử C trong 44 g CO 2
A. 2 mol B. 1 mol C. 0,5 mol D. 1,5 mol
Câu 16: Số mol của 19,6 g H 2 SO 4
A. 0,2 mol B. 0,1 mol C. 0,12 mol D. 0,21 mol
Câu 17: Cho m Ca = 5 g, m CaO = 5,6 g. Kết luận nào sau đây là đúng
A. n Ca > n CaO B. n Ca < n CaO C. n Ca = n CaO D. không xác định được
P/s :nCa > nCaO
Câu 18: Cho n N2 = 0,9 mol; m Fe = 50,4 g. Kết luận nào sau đây về N 2 và Fe là đúng
A. Cùng khối lượng B. Cùng thể tích C. Cùng số mol D.m Fe < m N2
Câu 19: Phải cần bao nhiêu mol nguyên tử C để có 2,4.10 23 nguyên tử C
A. 0,5 mol B. 0,55 mol C. 0,4 mol D. 0,45 mol
Câu 20: Dãy các chất đều là oxit là
A. PbO, NaOH, CO 2 , FeO B. PbO, Na 2 O, CaO, Al 2 O 3
C. NO 2 , HCl, SO 2 , P 2 O 5 D. FeO HCl, SO 2 , NaOH
Câu 1: Nếu 2 chất khí khác nhau nhưng đo ở cùng nhiệt độ và áp suất thì chúng có
A. Cùng khối lượng B. Cùng số mol
C. Cùng tính chất hóa học D. Cùng tính chất vật lí
Câu 2: Tính số nguyên tử của 1,8 mol Fe
A. 10,85.10 23 nguyên tử B. 10,8.10 23 nguyên tử
C. 11.10 23 nguyên tử D. 1,8.10 23 nguyên tử
Câu 3: Khối lượng mol chất là
A. Là khối lượng ban đầu của chất đó
B. Là khối lượng sau khi tham gia phản ứng hóa học
C. Bằng 6.10 23
D. Là khối lượng tính bằng gam của N nguyên tử hoặc phân tử chất đó
Câu 4: Cho biết 1 mol chất khí ở điều kiện bình thường có thể tích là
A. 2,24 l B. 0,224 l C. 24 l D. 22,4 ml
Câu 5: Tính thể tích ở đktc của 2,25 mol O 2
A. 22,4 l B. 24 l C. 5,04 l D. 50,4 l
Câu 6: Số mol của H 2 ở đktc biết V= 5,6 l
A. 0,25 mol B. 0,3 mol C. 0,224 mol D. 0,52 l
Câu 7: Thể tích mol là
A. Là thể tích của chất lỏng B. Thể tích của 1 nguyên tử nào đó
C. Thể tích chiếm bởi N phân tử của chất khí đó D. Thể tích ở đktc là 22,4 l
Câu 8: Số mol của kali 1,5.10 23 nguyên tử kali là
A. 1 mol B. 1,5 mol C. 0,5 mol D. 0,25 mol
Câu 9: Chọn đáp án sai:
A. Khối lượng của N phân tử CO 2 là 18 g
B. M H2 O = 18 g/mol
C. 1 mol O 2 ở đktc là 24 l
D.Thể tích mol của chất khí phải cùng t 0 và áp suất
Câu 10: Ở đktc 8 mol N 2 cố thể tích là
A. 179,2 l B. 17,92 l C. 0,1792 l D. 1,792 l
Câu 11: Cho 2,3 g Na phản ứng hết với oxi, sau phản ứng thu được natri oxit.khối
lượng chất tạo thành la
A. 0,31 g B. 3 g C. 3,01 g D. 3,1 g
Câu 12: Cho sơ đồ phản ứng sau Fe + H 2 SO 4 → FeSO 4 + H 2 , biết m Fe = 15,12 g Thể
tích hiđro thu được là
A. 6,048 l B. 8,604 l C. 5,122 l D. 2,45 l
Câu 13: Số mol của 12g O 2 , 1,2 g H 2 , 14 g N 2 lần lượt là
A. 0,375 mol; 0,6 mol; 0,5 mol
B. 0,375 mol; 0,5 mol; 0,1 mol
C. 0,1 mol; 0,6 mol; 0,5 mol
D. O,5 mol; 0,375 mol; 0,3 mol
Câu 14: Ở đktc 96 (g) CH 4 có thể tích là
A. 134,4 l B. 0,1344 ml C. 13,44 ml D. 1,344 ml(cái này là lít mới đúng nha)
Câu 15: Số mol nguyên tử C trong 44 g CO 2
A. 2 mol B. 1 mol C. 0,5 mol D. 1,5 mol
Câu 16: Số mol của 19,6 g H 2 SO 4
A. 0,2 mol B. 0,1 mol C. 0,12 mol D. 0,21 mol
Câu 17: Cho m Ca = 5 g, m CaO = 5,6 g. Kết luận nào sau đây là đúng
A. n Ca > n CaO
B. n Ca < n CaO > cái này là j vậy
C. n Ca = n CaO
D. không xác định được
Câu 18: Cho n N2 = 0,9 mol; m Fe = 50,4 g. Kết luận nào sau đây về N 2 và Fe là đúng
A. Cùng khối lượng B. Cùng thể tích C. Cùng số mol D.m Fe < m N2
Câu 19: Phải cần bao nhiêu mol nguyên tử C để có 2,4.10 23 nguyên tử C
A. 0,5 mol B. 0,55 mol C. 0,4 mol D. 0,45 mol
Câu 20: Dãy các chất đều là oxit là
A. PbO, NaOH, CO 2 , FeO
B. PbO, Na 2 O, CaO, Al 2 O 3
C. NO 2 , HCl, SO 2 , P 2 O 5
D. FeO HCl, SO 2 , NaOH
Có mấy câu mk ko hiểu nghĩa bạn đọc và bình luận bên dưới mình giải sau nhé

Gọi công thức của hai hiđrocacbon là C n H 2 n , C m H 2 m với m > n > 2
Phương trình hoá học :
C n H 2 n + 3n/2 O 2 → n CO 2 + n H 2 O
C m H 2 m + 3m/2 O 2 → m CO 2 + m H 2 O
n hh = 8,96/22,4 = 0,4 mol
n C m H 2 m = 0,4/100 x 25 = 0,1 mol
n C n H 2 n = 0,4 - 0,1 = 0,3 mol
Theo phương trình hóa học: n H 2 O = n CO 2 = 40,6/44 = 0,9 mol
Vậy 8,96 lít hỗn hợp X có khối lượng:
m X = m C + m H = 0,9 x 12 + 0,9 x 2 = 12,6g
Ta có n CO 2 = 0,3n + 0,1m = 0,9 => 3n + m = 9
=> n = 2; m = 3. Công thức của 2 hidrocacbon C 2 H 4 và C 3 H 6
\(n_{NaOH}=\dfrac{14}{40}=0,35\left(mol\right)\\ n_{ZnO}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2\left(mol\right)\)