Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)Phản ứng sản xuất NH3 là phản ứng tỏa nhiệt, lượng nhiệt tỏa ra dùng để đốt nóng hỗn hợp N2 và H2 cho phản ứng tiếp tục xảy ra
=> Tiết kiệm nhiên liệu đốt cho quá trình phản ứng
b) N2(g) + 3H2(g) → 2NH3(g) ${\Delta _r},H_{298}^0$= -92,22 kJ
Ta có: -92,22 = 2 x ∆fH0298 (NH3) – 1 x ∆fH0298 (N2) - 3 x ∆fH0298 (H2)
=> -92,22 = 2 x ∆fH0298 (NH3) – 0 – 0
=> ∆fH0298 (NH3) = -46,11 kJ

- Xét X là F:
CH4(g) + F2(g) → CH3F(g) + HF(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (F2) - 1 x Eb (HF) - x Eb (CH3F)
∆rH0298 = 1 x 4EC-H + 1 x EF-F - 1 x EH-F - 1 x (3EC-H + EC-F)
∆rH0298 = 1x4 x414 + 1x159– 1x565 - 1x(3x414 + 1x485)= -477kJ
- Xét X là Cl:
CH4(g) + Cl2(g) → CH3Cl(g) + HCl(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (Cl2) - 1 x Eb (HCl) - x Eb (CH3Cl)
∆rH0298 = 1 x 4EC-H + 1 x ECl-Cl - 1 x EH-Cl - 1 x (3EC-H + EC-Cl)
∆rH0298 = 1x4 x414 + 1x243– 1x431 - 1 x(3x414 + 1x339)= -113kJ
- Xét X là Br:
CH4(g) + Br2(g) → CH3Br(g) + HBr(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (Br2) - 1 x Eb (HBr) - x Eb (CH3Br)
∆rH0298 = 1 x 4EC-H + 1 x EBr-Br - 1 x EH-Br - 1 x (3EC-H + EC-Br)
∆rH0298 = 1x4 x414 + 1x193– 1x364 - 1 x(3x414 + 1x276)= -33kJ
- Xét X là I:
CH4(g) + I2(g) → CH3I(g) + HI(g)
∆rH0298 = 1 x Eb (CH4) + 1 x Eb (I2) - 1 x Eb (HI) - x Eb (CH3I)
∆rH0298 = 1 x 4EC-H + 1 x EI-I - 1 x EH-I - 1 x (3EC-H + EC-I)
∆rH0298 = 1x4 x414 + 1x151– 1x297 - 1 x(3x414 + 1x240)= 28kJ
=> Từ F đến I, tính phi kim giảm dần nên khả năng tham gia phản ứng giảm dần

còn cái ý trung hòa axit dư ở câu 2b thì cần phải có CM của axit sulfuric à
\(CH_4+2O_2\rightarrow CO_2+2H_2O\)
a a (mol)
\(C_2H_4+3O_2\rightarrow2CO_2+2H_2O\)
b 2 b (mol)
\(n_G=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
n\(_{CO_2}=\dfrac{48,4}{44}=1,1\left(mol\right)\)
gọi số mol của CH\(_4\) trong G là a;C\(_2H_4\) là b,ta có hệ phương trình:
\(\left\{{}\begin{matrix}a+2b=1,1\\a+b=0,8\end{matrix}\right.\)
\(\left\{{}\begin{matrix}a=0,5\\b=0,3\end{matrix}\right.\)
\(V_{CH_4}=22,4.0,5=11,2\left(g\right)\)
\(\rightarrow\%V_{CH_4}=\dfrac{11,2}{17,92}.100=62,5\%\)
\(\%V_{C_2H_4}=100\%-62,5\%=37,5\%\)
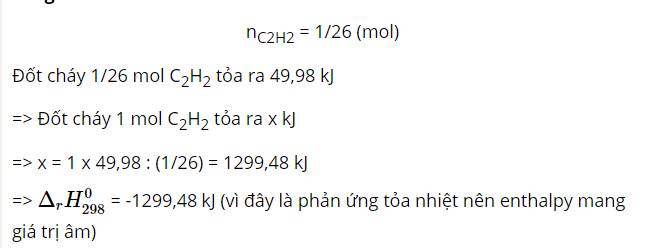
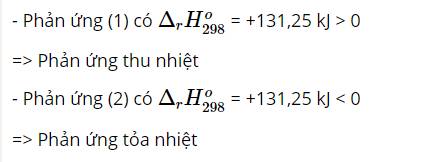
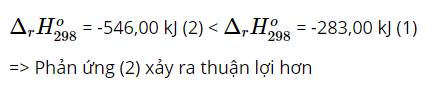
- Xét phản ứng đốt cháy 1 mol C2H4:
C2H4 (g) + 3O2 (g) → 2CO2 (g)+ 2H2O (g)
∆fH0298 = 2 x ∆fH0298 (CO2) + 2 x ∆fH0298 (H2O) - 3 x ∆fH0298 (O2) - 1 x ∆fH0298 (C2H4)
= -393,5 x 2 + -241,8 x 2 – 3 x 0 – 1 x 52,4 = -1323 kJ.mol-1
- Xét phản ứng đốt cháy 1 mol C2H6:
C2H6 (g) + 7/2 O2 (g) → 2CO2 (g)+ 3H2O (g)
∆fH0298 = 2 x ∆fH0298 (CO2) + 3 x ∆fH0298 (H2O) - 7/2 x ∆fH0298 (O2) - 1 x ∆fH0298 (C2H6)
= -393,5 x 2 + -241,8 x 3 –7/2 x 0 – 1 x -84 = -1428,4 kJ.mol-1
- Xét phản ứng đốt cháy 1 mol CO:
CO(g) + ½ O2 (g) → CO2(g)
∆fH0298 = 1 x ∆fH0298 (CO2) – 1/2 x ∆fH0298 (O2) - 1 x ∆fH0298 (CO)
= -393,5 x 1 – 1/2 x 0 – 1 x -110,5 = -283 kJ.mol-1