Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D.
Thí nghiệm tạo ra muối sắt (II) là: (2); (4); (5).
(1) 2Fe + 3Cl2 → 2FeCl3.
(2) Fe + S → FeS.
(3) 3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O.
(4) Fe + Fe2(SO4)3 → 3FeSO4.
(5) Fe + H2SO4 loãng → FeSO4 + H2.

Đáp án D.
Thí nghiệm tạo ra muối sắt (II) là: (3); (4); (5).
(1) 2Fe + 3Cl2 → t o 2FeCl3.
(2) 3FeO + 10HNO3 → 3Fe(NO3)3 + NO + 5H2O.
(3) Fe + Fe2(SO4)3 → 3FeSO4.
(4) Fe + H2SO4 → FeSO4 + H2.
(5) Fe + S → t o FeS.

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O

Áp dụng ĐLBTKL:
mhh = mX + mY + mCO3 = 10 g; mA = mX + mY + mCl = 10 - mCO3 + mCl.
số mol CO3 = số mol CO2 = 0,03 mol.
Số mol Cl = 2 (số mol Cl2 = số mol CO3) (vì muối X2CO3 tạo ra XCl2, Y2CO3 tạo ra 2YCl3).
Do đó: mA = 10 - 60.0,03 + 71.0,03 = 10,33g.

-\(n_{Fe}=\frac{11,2}{56}=0,2mol\) \(n_{Al}=\frac{m}{27}mol\) |
-khi thêm \(Fe\) vào cốc đựng \(HCl\) ( cốc A ) có phản ứng: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) 0,2 0,2 |
theo định luật bảo toàn khối lượng, khối lượng cốc \(HCl\) tăng thêm: \(11,2-\left(0,2.2\right)=10,8g\) |
khi thêm \(Al\) vào cốc đựng dd \(H_2SO_4\) có phản ứng: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\) \(\frac{m}{27}mol\) \(\rightarrow\) \(\frac{3.m}{27.2}mol\) |
| khi cho \(m\) gam \(Al\) vào cốc B, cốc B tăng thêm : \(m-\frac{3.m}{27.2}mol\) |
để cân thăng bằng, khối lượng ở cốc đựng \(H_2SO_4\) cũng phải tăng thêm 10,8g.Có: \(m-\frac{3.m}{27.2}.2=10,8\)
|
| giải ra được \(m=\) \(\left(g\right)\) |
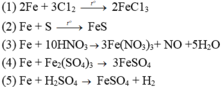


Chọn D.
(a) 2Fe + 3Cl2 → t ° 2FeCl3
(b) Fe + S → t ° FeS
(c) 3FeO + 10HNO3 ® 3Fe(NO3)3 + NO + 5H2O
(d) Fe + Fe2(SO4)3 ® 2FeSO4
(e) Fe + H2SO4 ® FeSO4 + H2
(g) Fe + 3AgNO3 ® Fe(NO3)3 + 3Ag