Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án: A
M có số hiệu nguyên tử là 19 nên điện tích hạt nhân nguyên tử M là 19+. M thuộc chu kỳ 4 nên có 4 lớp electron trong nguyên tử; M thuộc nhóm I nên lớp ngoài cùng có 1 electron. M đứng ở đầu chu kỳ nên là kim loại mạnh

Đề bài cho hỗn hợp X gồm hai khí là methane (CH4) và ethylene (C2H4). Hỗn hợp này có tỉ khối so với hydrogen (H2) bằng 10.
- Bước 1: Tính khối lượng mol trung bình của hỗn hợp X (MX)
Tỉ khối của hỗn hợp X so với hydrogen được tính bằng công thức: dX/H2=MH2MX.
Trong đó, MH2=2 g/mol.
Ta có: 10=2MX⇒MX=10×2=20 g/mol.
- Bước 2: Gọi thành phần phần trăm thể tích của từng khí trong hỗn hợp
Giả sử trong 1 mol hỗn hợp X, số mol của CH4 là x và số mol của C2H4 là y.
Ta có: x+y=1 (1)
Khối lượng mol trung bình của hỗn hợp X được tính bằng công thức: MX=nCH4+nC2H4nCH4⋅MCH4+nC2H4⋅MC2H4.
MCH4=12+4=16 g/mol.
MC2H4=12×2+4=28 g/mol.
Thay vào công thức ta có: 20=x+yx⋅16+y⋅28=116x+28y (2)
Từ (1) và (2) ta có hệ phương trình:
x+y=1
16x+28y=20
Giải hệ phương trình này, ta được: x=32 và y=31.
Điều này có nghĩa là trong hỗn hợp X, số mol của CH4 chiếm 32 và số mol của C2H4 chiếm 31.
- Bước 3: Tính tổng số mol của hỗn hợp X
Thể tích của hỗn hợp X ở điều kiện tiêu chuẩn (đktc) là 3,7185 lít.
Số mol của hỗn hợp X là: nX=24.79V=24.793.7185=0.15 mol.
(Lưu ý: Nếu đề bài cho ở điều kiện tiêu chuẩn cũ (0 độ C, 1 atm) thì V = 22.4, nhưng theo quy ước quốc tế mới, 1 bar và 25 độ C thì V = 24.79. Đề bài không nói rõ nên ta chọn chuẩn mới là 24.79).
- Bước 4: Tính số mol C2H4 trong hỗn hợp X
Từ kết quả ở bước 2, ta biết số mol C2H4 chiếm 31 tổng số mol.
nC2H4=nX×y=0.15×31=0.05 mol.
- Bước 5: Tính số mol Br2 đã phản ứng
Khi hỗn hợp X cho qua dung dịch Br2 dư, chỉ có ethylene (C2H4) phản ứng vì nó có liên kết đôi (C=C). Methane (CH4) là ankan nên không phản ứng với Br2.
Phương trình phản ứng:
C2H4+Br2→C2H4Br2
Theo phương trình, tỉ lệ mol là 1:1, vậy:
nBr2=nC2H4=0.05 mol.
Kết luận
Số mol Br2 đã tham gia phản ứng là 0,05 mol.

Tổng điện tích hạt nhân là : 31
\(p_X+p_Y=31\left(1\right)\)
Hai nguyên tố nằm ở hai nhóm kế tiếp nhau cùng chu kì nên :
\(p_X-p_Y=1\left(2\right)\)
\(\left(1\right),\left(2\right):p_X=16,p_Y=15\)
Y: Ô 16 , Chu kì 3 , Nhóm VIA
X : Ô 15 , Chu kì 3 , Nhóm VA

mAgNO3=500*4/100=20g
mAgNO3giảm=20*68/100=17g
=>nAgNO3=17/170=0.1 mol
PTHH: Cu + 2AgNO3 ------> Cu(NO3)2 + 2Ag
0.05 0.1 0.05 0.1
mCu = 0.05*64=3,2g
mAg =0.1*108= 10,8g
=>khối lượng vật là 5 + 10,8 - 3,2 = 12,6 g
b) từ từ anh làm nhé!!@
nAgNO3 = \(\frac{500.4\%}{170}\) = 2/17 mol
nCu = 0,078125 mol
Cu + 2AgNO3 => Cu(NO3)2 + 2Ag
0,05 <----0,1---------0,05-------> 0,1
m AgNO3 giảm = mAgNO3 pư = 2/17 . 85% = 0,1 mol
ta có m kim loại tăng = 0,05( 216-64) = 7,6
=> m vật = 5+ 7,6 = 12,6 (g)
nAgNO3 dư = \(\frac{2}{17}\) - 0,1 = \(\frac{3}{170}\)
mdd = 5+ 500 - 12,6 = 492,4
C% AgNO3 dư = \(\frac{\frac{3}{170}.170}{492,4}\) .100% = 0,609%
C% Cu(NO3)2 = \(\frac{0,05.188}{492,4}\) .100% = 1,9%


Cấu hình của Y: 1s22s22p4
=> Y có 2 lớp e
=> Y có số electron lớp ngoài cùng là 6
=> Y có điện tích hạt nhân là 8+
Chọn 1,3,5
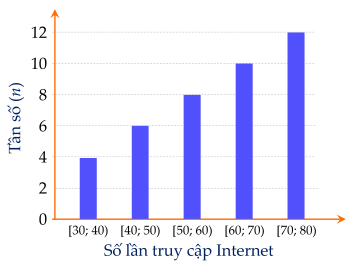


tần số tương đối ghép nhóm của nhóm [60,70) là 10%.
Tỉ lệ điều tra số lần truy cập Internet của 40 người từ 60 đến dưới 70 là 10 : 40 x 100% =25%.