Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
+ Khi cho Y tác dụng với KNO 3 , H 2 SO 4 thu được 2 khí có tỉ khối so với H 2 là 8 và có một khí hóa nâu. Suy ra 2 khí là NO và H 2 . Như vậy, trong Y có Fe và Z không chứa O 2 .
+ Sơ đồ phản ứng
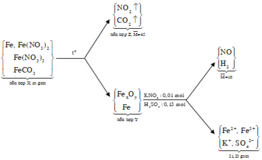
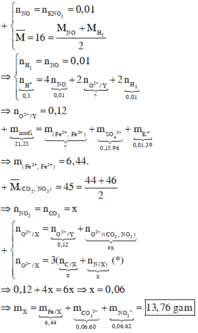

Quy đổi Y thành Fe và O ta có sơ đồ:
Sơ đồ ta có:
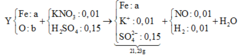
+ Bảo toàn khối lượng muối ta có nFe = a = 0,115 mol.
+ PT theo H+: 0,3 = 2nO + 4nNO + 2nH2.
⇒ nO = 0,12 mol.
● Quy đổi X thành Fe, NO3 và CO3 ta có:
Nung X ta có sơ đồ:
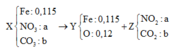
+ Từ MZ = 45 ⇒ nNO2 = nCO2
Û a = b Û a – b = 0 (1)
⇒ Bảo toàn oxi ta có: a + b = 0,12 mol (2)
+ Giải hệ (1) và (2) ⇒ nNO3 = nCO3 = 0,06 mol.
⇒ m = 0,115×56 + 0,06×(62+60) = 13,76
Đáp án A

Đáp án D
Hỗn hợp khí có M = 2.8 = 16
=> có H2 và NO
=> nH2 = nNO, vì có H2
=> 0,01 mol KNO3 hết cho 0,01 mol NO
=> nH2 = 0,01
Trong muối có:
Fe x mol, K+ 0,01 mol, SO4 2- 0,15 mol
m Muối = 56x + 39.0,01 + 96.0,15 = 21,23
=> x = 0,115
=> mFe = 6,44
=> Khí Z gồm NO2 và CO2 có M = 45
=> nNO2 = nCO2 = a
=> trong X có: Fe 0,115 mol, NO3- a mol , CO32- a mol
=> nO = 6a mol ( bảo toàn mol O trong CO3 và NO3)
=> trong Y có 0,115 mol Fe và 2a mol O ( giảm 4a do tạo khí NO2 và CO2)
NO3-+3e+4 H+->NO + 2 H2O
0,01 0,04 0,01
2 H+ + 2e -> H2
0,02 0,01
2 H+ + O -> H2O
4a 2a
nH+ = 0,04 + 0,02 + 4a = 2.0,15
=> a = 0,06
m X = mFe + mNO3 + mCO3
= 6,44 + 62.0,06 + 60.0,06
= 13,76

Vì ta có thể tính được ngay số mol của N2 và H2 và đây cũng là dự kiện mấu chốt để tìm m với dạng toàn này nên đầu tiên ta tìm số mol của N2 và H2 bằng cách: đặt nN2 và H2 lần lượt là x, y. Ta được: x + y = 0,025
tỉ khối so với H2: 28x + 2y/ 2(x + y) = 11,4 (với x + y = 0,025)
=> x = 0,02; y = 0,005
Sử dụng bảo toàn electron: số mol electron nhường = số mol electron nhận thì: 2nMg > ***N2 + 2nH2 nên phản ứng có tạo NH4Cl
quá trình oxi hóa: Mg - 2e -----> Mg2+
quá trình khử: 2NO3- -10e ----> N2 (N(+5) -5e ----> N(0))
NO3- -8e ------> NH4+ (n(+5) - 8e ---> N(-3))
2H+ -2e ---> H2
Vậy 2.0,124 = 0,025.10 + 0,005.2 + 8nNH4+ => nNH4+ = 0,01
m = mMgCl2 + mNH4Cl = 0,145.95 + 0,01.53,5 = 14,31 gam
mol Mg = 0,145 ==> mol e nhường = 0,29 ==> mol NH4+ = 0,01
2 NO3- + 10e + 12 H+ ----> N2 + 6 H2O
0,04-------0,2------0,24-------0,02
NO3- + 8e + 10 H+ ----> NH4+ + 3 H2O
0,01----0,08------0,1-------0,01
2 H+ + 2e ----> H2
0,01----0,01------0,005
mol HCl = mol Cl- = mol H+ = 0,35
mol KNO3 = mol K+ = mol NO3- = 0,05
muối gồm : Mg2+ = 0,145 mol, NH4+ = 0,01 mol, K+ = 0,05 và mol Cl- = 0,35
khối lượng muối = 24*0,145 + 39*0,05 + 35,5*0,35 = 18,035

Bài 1:
A + Cl2 → ACl2 (1)
Fe + ACl2 → FeCl2 + A (2)
x x x (mol)
gọi số mol của Fe phản ứng với một số mol của ACl2 là x
khối lương thanh sắt sau phản ứng là:11,2 - 56x + xMA = 12
=> x =
Ta có:
= 0,25.0,4 = 0,1 (mol)
=> MA = 64 g/mol; Vậy kim loại A là Cu
= nCu =
= 0,2 (mol) =>
= 0,5M
bài 2:
(C17H35COO)3C3H5 + 3NaOH -> 3 C17H35COONa + C3H5(OH)3
890 kg 918 kg
x kg 720 kg
=> x = 698,04 kg.
 với các chất sau:
với các chất sau:
Đáp án A
Do vậy NO3- trong Y phản ứng hết.
Giải được số mol NO, H2 thu được đều là 0,01 mol. (Bảo toàn N và đường chéo)
Đặt a, b là số mol của ion Fe2+, Fe3+ trong muối trung hòa. Gọi x là số mol O trong rắn Y.
Bảo toàn e:
Bảo toàn điện tích:
=>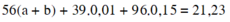
Giải được: a=0,055; b=0,06; x=0,12.
Quy đổi hỗn hợp X về Fe 0,115 mol (bảo toàn Fe), NO3 u mol và CO3 v mol.
Khí Z gồm CO2 và NO2.
Bảo toàn O: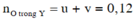
Dựa vào tỉ khối của Z là 45 áp dụng đường chéo giải được u=v0,06.