Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

6: A
7: A
K2O + H2O --> 2KOH
BaO + H2O --> Ba(OH)2
CaO + H2O --> Ca(OH)2
Na2O + H2O --> 2NaOH
8: C
- Cho 3 chất rắn tác dụng với dd NaOH
+ Chất rắn tan, sủi bọt khí: Al
2Al + 2H2O + 2NaOH --> NaAlO2 + 3H2
+ Chất rắn không tan: Fe, Cu
- Cho 2 chất rắn còn lại tác dụng với dd H2SO4
+ Chất rắn tan, sủi bọt khí: Fe
Fe + H2SO4 --> FeSO4 + H2
+ Chất rắn không tan: Cu
9: D

Do A, B là hợp chất hữu cơ đơn chức, có khả năng tác dụng với NaOH
=> trong phân tử A,B chứa 2 nguyên tử oxi
=> MA = MB = 32 . 100/21,621= 148 g/mol
=> CTPT của A,B là C9H8O2 .
TN1: nA + nB = 0,74/148=5.10-3
Mà m sản phẩm=1,54
=> cả A,B đều có khả năng tham gia phản ứng cộng với dung dịch Br2 theo tỉ lệ mol 1:1
=> A,B chứa 1 nối đôi C=C trong phân tử ( không phải este của phenol)
TN5: Do A,B bị oxi hóa bởi KMnO4 tạo ra C7H8O2 và CO2 => A,B chứa vòng benzen
TN2: nA + nB= 2,22/148=0,015 mol
Do hỗn hợp X có khả năng tác dụng với NaHCO3 => hỗn hợp có chứa axit
=> naxit= nCO2 = 5.10-3 => neste= 0,01 mol
TN3: trong 4,44 gam hỗn hợp naxit = 0,01 mol, neste= 0,02
=> mmuối sinh ra từ este = 4,58 – 0,01 . MC8H7COONa= 2,88
=> Mmuối sinh ra từ este = 144 g/mol.
=> CT muối sinh ra từ este là: C6H5COONa
=> CTCT A,B là: C6H5COOC2H3 và C6H5-CH=CH-COOH
=> ( loại trường hợp axit có CT C6H5-C(COOH)=CH2 vì axit này không bị oxi hóa tạo C6H5COONa và CO2)
PTHH:
C6H5COOC2H3+ 2KMnO4 +3 H2SO4 → C6H5COOH + 2CO2 + K2SO4 + 2MnSO4 + 4H2O
C6H5-CH=CH-COOH +2 KMnO4 + 3H2SO4 →C6H5COOH + 2CO2 + K2SO4 + 2MnSO4 + 4H2O.

a)
$CH_3COOH + NaHCO_3 \to CH_3COONa + CO_2 + H_2O$
b)
n NaHCO3 = n CH3COOH = 100.12%/60 = 0,2(mol)
m dd NaHCO3 = 0,2.84/8% = 210(gam)
c)
n CO2 = n CH3COOH = 0,2(mol)
=> V CO2 = 0,2.22,4 = 4,48(lít)
d)
m dd = m dd CH3COOH + m dd NaHCO3 - m CO2 = 100 + 210 - 0,2.44 = 301,2(gam)
C% CH3COONa = 0,2.82/301,2 .100% = 5,44%

Câu 1.
a) Oxit + nước -------> dung dịch axit:
CO2 + H2O -----> H2CO3
SO2 + H2O -----> H2SO3
b) Oxit + nước -------> dung dịch bazơ:
Na2O + H2O -----> 2NaOH
CaO + H2O -----> Ca(OH)2
c) Oxit + dung dịch axit ----> Muối + nước:
1. Na2O + 2HCl -----> 2NaCl2 + H2O
2. CaO + 2HCl -----> CaCl2 + H2O
3. CuO + 2 HCl -----> CuCl2 + H2O
d) Oxit + dung dịch bazơ ----> Muối + nước:
CO2 + 2NaOH → Na2CO3 + H2O
SO2 + 2NaOH → Na2SO3 + H2O
Câu 2.
Số mol của CuO là:
\(n_{CuO}=\frac{1,6}{80}=0,02\left(mol\right)\)
\(\rightarrow n_{H_2SO_4}=\frac{m_{dd}\cdot C\%}{M\cdot100\%}=\frac{100\cdot20\%}{98\cdot100\%}\approx0,2\left(mol\right)\)
a) PTHH:
CuO + H2SO4 ----> CuSO4 + H2O
1mol____1mol
0,02______0,2mol
Lập tỉ lệ: \(\frac{0,02}{1}< \frac{0,2}{1}\)
\(\Rightarrow\) CuO hết, H2SO4 dư
- Theo pt: \(n_{CuSO_4}=n_{CuO}=0,02\left(mol\right)\)
\(\Rightarrow m_{CuSO_4}=0,02\cdot160=3,2\left(g\right)\)
-Theo pt: \(n_{H_2SO_4\left(td\right)}=n_{CuO}=0,02\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2\cdot0,02=0,18\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(dư\right)}=0,18\cdot98=17,64\left(g\right)\)
Áp dụng ĐLBTKL để tính khối lượng dung dịch thu được sau phản ứng. Ta có:
mCuO + m\(ddH_2SO_4\) + mdd(sau pư)
\(\Rightarrow\) mdd(sau pư) = 1,6 + 100 = 101,6 (g)
b) Nồng độn phần trăm của CuSO4:
\(C\%_{CuSO_4}=\frac{m_{CuSO_4}\cdot100\%}{m_{dd}\left(sau\right)}=\frac{3,2\cdot100\%}{101,6}=3.15\%\)
Nồng độ phần trăm của H2SO4 dư:
\(C\%_{H_2SO_4}=\frac{m_{H_2SO_4\left(dư\right)}\cdot100\%}{m_{dd}\left(sau\right)}=\frac{17,64\cdot100\%}{101,6}=17,36\%\)
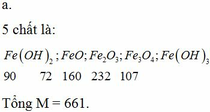
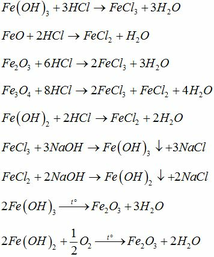
hình như là các muối của Al vàZn
AlCl3.ZnSO4,Cr(NO3)3,Be3(PO4)2