Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`#3107.101107`
a. Sửa đề: Hãy cho biết khối lượng nguyên tử của mỗi nguyên tố có trong phân tử đó.
- Trong phân tử \(\text{SO}_2\) gồm 2 nguyên tử, nguyên tử S và O
`=>` NTK của S là `32` amu, NTK của phân tử O là `16` amu
b.
Khối lượng phân tử của SO2 là:
\(32+16\cdot2=64\left(\text{amu}\right)\)
c.
Số `%` của S có trong SO2 là:
\(\text{%S }=\dfrac{32\cdot100}{64}=50\left(\%\right)\)
Số `%` của O2 có trong SO2 là:
\(\text{%O = 100%}-\text{50% = 50%}\)
Vậy:
a. S: `32` amu, O: `16` amu
b. PTK của SO2 là `64` amu
c. \(\text{%S = 50%; %O = 50%.}\)

klpt : Fe2O3 là : 56.2+16.3=160(amu)
%Fe = \(\dfrac{56.2}{160}\) . 100% = 70%
%O = \(\dfrac{16.3}{160}\) . 100% = 305
Làm ơn tick cho mk

Gọi ct chung: \(H_xO_y\)
\(K.L.P.T=1.x+16.y=18< amu>.\)
\(\%H=\dfrac{1.x.100}{18}=11,11\%\)
\(H=1.x.100=11,11.18\)
\(H=1.x.100=199,98\)
\(1.x=199,98\div100\)
\(1.x=1,9998\)
\(\Rightarrow\)\(x=1,9998\) làm tròn lên là 2
vậy, có 2 nguyên tử H trong phân tử \(H_xO_y\)
\(\%O=\dfrac{16.y.100}{18}=88,89\%\)
\(\Rightarrow y=1,00...\) làm tròn lên là 1 (cách làm tương tự).
Vậy, có 1 nguyên tử O trong phân tử trên
\(\Rightarrow CTHH:H_2O.\)

Trong phân tử \(CO\left(NH_2\right)_2\) có 2 nguyên tử N.
Trong phân tử \(\left(NH_4\right)_2SO_4\) có 2 nguyên tử N.
Trong phân tử \(NH_4NO_3\) có 2 nguyên tử N.
Trong phân tử \(Ca\left(NO_3\right)_2\) có 2 nguyên tử N.
Vậy trong cùng 1 phân tử, các chất trên đều cùng số nguyên tử N, vậy nên bác nông dân chọn loại nào cũng được.
b phải tính phần trăm nito trong đó chứ ko p tính số nguyên tử :))

`@` `\text {MgO}`
\(\text{PTK = 24 + 16 = 40 < amu>}\)
\(\%\text{O}=\dfrac{16\cdot100}{40}=40\%\)
Vậy, khối lượng `%` của `\text {O}` trong `\text {MgO}` là `40%`
`@` `\text {Fe}_2 \text {O}_3`
\(\text{PTK = }56\cdot2+16\cdot3=160\text{ }< \text{amu}\text{ }>\)
\(\%\text{Fe}=\dfrac{56\cdot2\cdot100}{160}=70\%\)
Vậy, khối lượng `%` của `\text {Fe}` trong `\text {Fe}_2 \text {O}_3` là `70%`

Ta có:
MH = 1 amu
MO = 16 amu
Ta có:
\(M_{H_2O}=1
.
2+16=18\left(amu\right)\)
\(\%m_H=\dfrac{M_{H_2O}}{M_{H_2}}
.
100\%=9\%\)
\(\%m_O=100\%-9\%=91\%\)
=> Nhận định trên là sai.
Trong phân tử nước gồm: 1 nguyên tử O và 2 nguyên tử H
Ta có: Khối lượng của nguyên tố O trong nước là:
mO = 1 x 16 amu = 16 amu
Khối lượng của nguyên tố H trong nước là:
mH = 2 x 1 amu = 2 amu
=> Khối lượng phân tử nước là: Mnước = 16 + 2 = 18 amu
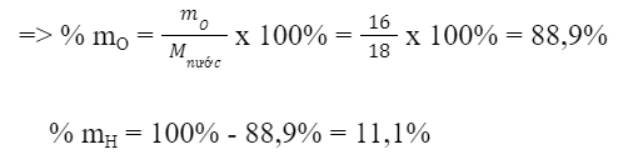
=> Ý kiến: Phần trăm khối lượng của H trong nước gấp 2 lần phần trăm khối lượng O là sai
A. Nước (H2O):
- Khối lượng phân tử của H2O = 2 . 1 (H) + 16 (O) = 18 g/mol.
- Phần trăm khối lượng của H trong H2O = (2 . 1/18) . 100% = 11,11%.
- Phần trăm khối lượng của O trong H2O = (16/18) . 100% = 88,89%.
B. Methane (CH4):
- Khối lượng phân tử của CH4 = 12 (C) + 4 . 1 (H) = 16 g/mol.
- Phần trăm khối lượng của C trong CH4 = (12/16) . 100% = 75%.
- Phần trăm khối lượng của H trong CH4 = (4 . 1/16) . 100% = 25%.