Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Mg+H_2SO_4->MgSO_4+H_2\\ 2KClO_3-^{t^o}>2KCl+3O_2\\ 3H_2+Fe_2O_3->2Fe+3H_2O\\ 4Al+3O_2-^{t^o}>2Al_2O_3\\ CH_4+2O_2-^{t^o}>CO_2+2H_2O\\ O_2+S-^{t^o}>SO_2\\ H_2+CuO-^{t^o}>Cu+H_2O\\ 2KMnO_4-^{t^o}>K_2MnO_4+MnO_2+O_2\\ Zn+2HCl->ZnCl_2+H_2\\ 4P+5O_2-^{t^o}>2P_2O_5\)
Đốt cháy hoàn toàn 5,4 g kim loại nhôm Al trong khí oxi. a. Tính thể tích khí oxi (đktc) cần dùng cho phản ứng. b. Tính khối lượng KClO3 cần dùng để điều chế lượng oxi trên.

1)
3Fe + 2O2 -to-> Fe3O4
C + O2 -to-> CO2
4P + 5O2 -to-> 2P2O5
4Al + 3O2 -to-> 2Al2O3
2Cu + O2 -to-> 2CuO
2Zn + O2 -to-> 2ZnO
S + O2 -to-> SO2
4Na + O2 -to-> 2Na2O
2Ba + O2 -to-> 2BaO
CH4 + 2O2 -to-> CO2 + 2H2O
C2H5OH + 3O2 -to-> 2CO2 + 3H2O
NO + 1/2O2 -to-> NO2
CO + 1/2O2 -to-> CO2
b)
2KClO3 -to-> 2KCl + 3O2
2KMnO4 -to-> K2MnO4 + MnO2 + O2
\(a)\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ C + O_2 \xrightarrow{t^o} CO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ 2Zn + O_2 \xrightarrow{t^o} 2ZnO\\ S + O_2 \xrightarrow{t^o} SO_2\\ 4Na + O_2 \xrightarrow{t^o} 2Na_2O\\ 2Ba + O_2 \xrightarrow{t^o} 2BaO\)
\(CH_4 + 2O_2 \xrightarrow{t^o} CO_2 + 2H_2O\\ C_2H_5OH + 3O_2 \xrightarrow{t^o} 2CO_2 + 3H_2O\\ 2NO + O_2 \to 2NO_2\\ 2CO + O_2 \xrightarrow{t^o} 2CO_2\\ b)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\)

\(a,S+O_2\underrightarrow{t^o}SO_2\) ( hóa hợp )
\(b,2Al+3O_2\underrightarrow{t^o}2Al_2O_3\) ( hóa hợp )
\(c,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\) ( phân hủy )
\(d,2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\) ( phân hủy )
a) \(S+O_2\xrightarrow[]{t^0}SO_2\left(phản.ứng.hoá.hợp\right)\)
b)\(4Al+3O_2\xrightarrow[t^0]{}2Al_2O_3\left(phản.ứng.hoá.hợp\right)\)
c) \(2KMnO_4\xrightarrow[t^0]{}K_2MnO_4+MnO_2+O_2\left(phản.ứng.phân.huỷ\right)\)
d)\(2KClO_3\xrightarrow[t^0]{}2KCl+3O_2\left(phản.ứng.phân.huỷ\right)\)

a)Fe2O3 → Fe →FeCl3 → FeCl2 → Fe(OH)2→ FeSO4 →Fe(NO3)2
b)Fe2O3 + 3H2 2Fe + 3H2O
2Fe + 3Cl2 2FeCl3
2FeCl3 + Fe → 3FeCl2
FeCl2 + 2NaOH → Fe(OH)2 + NaCl2 Fe(OH)2 + H2SO4 → FeSO4 + 2H2O
FeSO4 + Ba(NO3)2 → BaSO4 + Fe(NO3)2

a)
2H2O-đp>2H2+O2
b) SO4 ??
c)
2KClO3-to>2KCl+3O2
S+O2-to>SO2
SO2+O2-to, V2O5>SO3
SO3+H2O->H2SO4
2Cu+O2-to>2CuO
CuO+H2SO4->CuSO4+H2O
d) KClO3 + 6HCl → 3Cl2 + KCl + 3H2O
Cl2+Cu-to>CuCl2
2H2O -> (điện phân) 2H2 + O2
2KClO3 -> (t°, MnO2) 2KCl + 3O2
S + O2 -> (t°) SO2
2SO2 + O2 -> (t°, V2O5) 2SO3
SO3 + H2O -> H2SO4
Cu + H2SO4 (đặc nóng) -> CuSO4 + H2
2Cu + O2 -> (t°) 2CuO
CuO + 2HCl -> CuCl2 + H2O

\(C+O_2\xrightarrow[]{t^o}CO_2\)
\(S+O_2\xrightarrow[]{t^o}SO_2\)
\(4P+5O_2\xrightarrow[]{t^o}2P_2O_5\)
\(H_2+\dfrac{1}{2}O_2\xrightarrow[]{t^o}H_2O\)
\(4Na+O_2\rightarrow2Na_2O\)
\(Mg+\dfrac{1}{2}O_2\xrightarrow[]{t^o}MgO\)
\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\)
\(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
\(Cu+\dfrac{1}{2}O_2\xrightarrow[]{t^o}CuO\)
\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
\(4FeS_2+11O_2\xrightarrow[]{t^o}2Fe_2O_3+8SO_2\)
\(C_2H_6O+3O_2\xrightarrow[]{t^o}2CO_2+3H_2O\)
C+ O2 -to-> CO2
S+ O2 -to-> SO2
2 Cl2 + 7 O2 -to-> 2 Cl2O7
4P +5 O2 -to-> 2 P2O5
4Al + 3 O2 -to-> 2 Al2O3
4 Na+ O2 -to-> 2 Na2O
Mg + 1/2 O2 -to-> MgO
3 Fe +2 O2 -to-> Fe3O4
4 FeS2 + 11 O2 -to,xt-> 8 SO2 + 2 Fe2O3
H2 + 1/2 O2 -to->H2O
2 Ag + 1/2 O2 -to-> Ag2O
C2H6O + 3 O2 -to-> 2 CO2 + 3 H2O
CH4 + 2 O2 -to-> CO2 + 2 H2O
Cu + 1/2 O2 -to-> CuO

\(C+O_2\underrightarrow{t^o}CO_2\)
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
\(4Al++3O_2\underrightarrow{t^o}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(2CO+O_2\underrightarrow{t^o}2CO_2\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(2Ba+O_2\underrightarrow{t^o}2BaO\)
\(C_6H_6+\dfrac{15}{2}O_2\underrightarrow{t^o}6CO_2+3H_2O\)
\(4K+O_2\underrightarrow{t^o}2K_2O\)

- Pư với O2:
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(CO+\dfrac{1}{2}O_2\underrightarrow{t^o}CO_2\)
\(SO_2+\dfrac{1}{2}O_2\underrightarrow{t^o,V_2O_5}SO_3\)
\(Ba+\dfrac{1}{2}O_2\underrightarrow{t^o}BaO\)
- Pư với H2:
\(CuO+H_2\underrightarrow{^o}Cu+H_2O\)
- Pư với H2O:
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O⇌H_2SO_3\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
chất tác dụn với O2
\(2SO_2+O_2\xrightarrow[]{}2SO_3\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(4Al+3O_2\xrightarrow[]{}2Al_2O_3\)
\(CH_4+2O_2\xrightarrow[]{}CO_2+2H_2O\)
\(2CO+O_2\xrightarrow[]{}2CO_2\)
tác dụng với H2
\(CuO+H_2\xrightarrow[]{}Cu+H_2O\)
\(Al_2O_3+3H_2\xrightarrow[]{}2Al+3H_2O\)
\(Na_2O+H_2\xrightarrow[]{}2Na+H_2O\)
tác dụng với H2O
\(2Al+3H_2O\xrightarrow[]{}Al_2O_3+3H_2\)
\(Ba+2H_2O\xrightarrow[]{}Ba\left(OH\right)_2+H_2\)
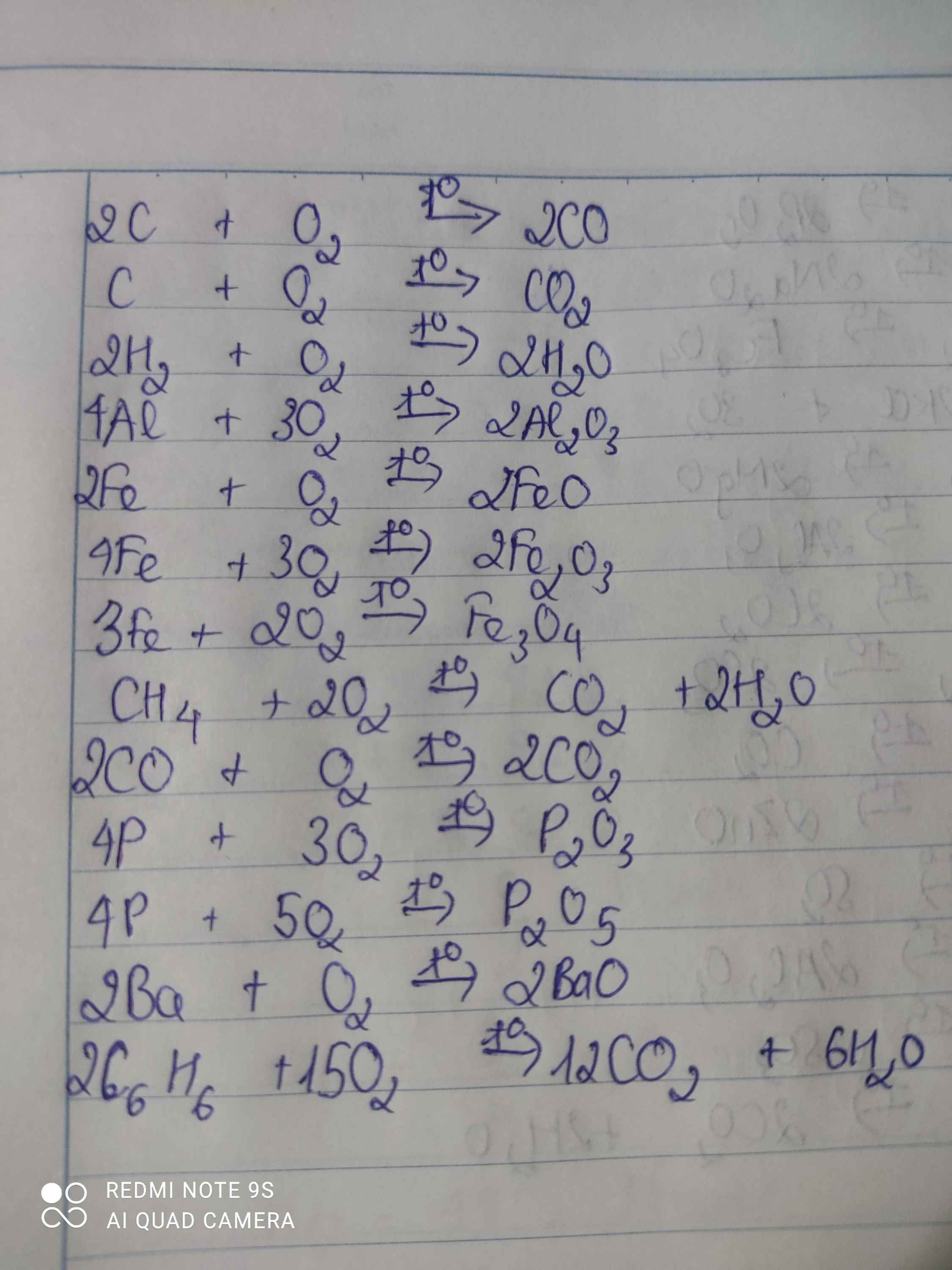
thiếu 4P+5O2---to->2P2O5