Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTPU

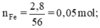
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (l)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)

Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
Bài giải:
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: = 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g

nAl=0,2mol
PTHH: 2Al+6HCl=>2AlCl3+3H2
0,2->0,6-> 0,2--->0,3
mAlCl3=0,2.133,5=26,7g
do H=90
=> mAlCl3=26.7/100.90=24,03g
VH2=0,3.22,4=6,72l
do H=90%
=> V H2=6,72/100.90=6,048l
nAl=5,4/27=0,2(mol)
voi h=90->nAl=0,2*90/100=0,18(mol)
2Al+6HCl->2AlCl3+3H2
TPT;nAlCl3=3nAl=0,18*3=0,54(mol)
->mAlCl3=0,54*133,5=72,09(g)
TPT;nH2=3/2nAl=0,18*3/2=0,12(mol)
->VH2=0,12*22,4=2,688(l)

a, PTHH : Fe + 2HCl -> FeCl2 + H2
nFe= 0,1(mol)
nHCl = 0, 411(mol)
Vì 0,1<0,411/2 => Fe hết , HCl dư
Theo PTHH , nFeCl2= 0,1 (mol) => m = 12,7 (g)
b , Theo PTHH, nH2 = 0,1(mol)=> V = 2,24(l)
c , Theo pthh , nHCl = 0,2(mol)=> nHCl dư = 0,211(mol) => m= 7,7015(g)
Đánh bằng phone bất tiện quá , nó lỗi hoài , có vài chỗ mik làm tắt , bạn thông cảm nha ^^
mình nghĩ bài này phải tính câu c trc vì biết đc chất nào dư thì mới tính theo PTHH đc :v
nFe = 5,6/56 = 0,1 mol
nHCl = 15/36,5 ≈ 0,4 mol
PTHH: Fe + 2HCl --> FeCl2 + H2
0,1 0,2 0,1 0,1
Tỷ lệ:
Fe HCl
nFe/1 nHCl/2
0,1/1 0,4/2
=> 0,1 < 0,2
=> HCl dư
nHCl dư = 0,4 - 0,2 = 0,2 mol
mHCl = 0,2. 36,5= 7,3g
Vì HCl dư nên đc tính theo Fe
Theo PTHH : nFeCl2 = nFe= 0,1 mol
=>mFeCl2= 0,1.127=12,7g
Theo PTHH: nH2= nFe = 0,1 mol
=>VH2= 0,1.22,4= 2,24 lít

a) 2C2H2 + 5O2 => 4CO2 + 2H2O
b) Fe2O3 + 3CO => 2Fe + 3CO2
c) 2CrCl3 + 3H2O => 6HCl + Cr2O3

2)M khí A= 17*2=34
cong thức tổng quát: HxSy
có:
M của H/ M khí A= % H
<=>H*x/M=5,88%
<=>1*x/34=5,88%
suy ra: x=2
=> y =1
công thức đúng là: H2S
1) Theo như SGK thì có 2,8g Fe, bạn ghi thiếu đề
a) nFe = 2,8 / 56 = 0,05 mol Phương trình hoá học: Fe + 2HCl -----> FeCl2 + H2 0, 05 mol 2.0,05 mol 0,05 mol Theo phương trình trên ta có nFe = nH = 0,05 VH2= 0,05 x 22,4 = 1,12 l. b) nHCl = 2nFe = 2 x 0,05 = 0,1 mol mHCl cần dùng: 0,1 x 36,5 = 3,65 g.

1 , CnH2n + \(\dfrac{3n}{2}\)O2 -> nCO2 + nH2O
2 , Fe2O3 + 3CO -> 2Fe + 3CO2
1)\(C_nH_{2n}\)+\(\dfrac{3n}{2}\)\(O_2\)->n\(CO_2\)+n\(H_2O\)
2)\(Fe_2O_3\)+3CO->3\(CO_2\)+2Fe

1. Cho td với quỳ tím
HBr làm quỳ tím hóa đỏ Ba(OH)2 làm quỳ tím hóa xanh CaCl2 làm quỳ tím ko đổi màu
a, Tìm thể tích khí H2 thu được \(\left(\text{đ}ktc\right)\)
- Phương trình hóa học :
Fe + 2HCl ➝ FeCl2 + H2
- Số mol Fe tham gia phản ứng :
nFe=\(\dfrac{2,8}{56}\)=0,05 mol
=Theo phương trình hóa học :
nH2=nFe=0,05 mol
Thể tích khí H2thu được ở đktc :
VH2= 22,4 . 0,05 = 1,12 lít
b , Khối lượng HCl cần dùng
- Theo phương trình hóa học :
nHCl=2nFe= 2 . 0,05 = 0,10 mol
- Khối lượng HCl cần dùng là :
mHCl=36,5 . 0,10 = 3,65 gam