Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. \(PTHH:2Cu+O_2\overset{t^o}{--->}2CuO\)
b. Áp dụng định luật bảo toàn khối lượng, ta có công thức về khối lượng là: \(m_{Cu}+m_{O_2}=m_{CuO}\)
c. Dựa vào câu b, suy ra:
\(m_{O_2}=m_{CuO}-m_{Cu}=12-9,6=2,4\left(g\right)\)
a. nCu = m/ M = 9.6/ 64 = 0.15 (mol)
PTHH 2Cu + O2 ➝ 2CuO
TL 2 1 2 (mol)
ĐB 0,15 0,075 0,15
b. m = n.M
c. mO2 = n. M = 0,075. (16.2) = 2,4 (mol)

a/ PTHH: 4P + 5O2 ===> 2P2O5
( Tính khối lượng oxi tham gia phản ứng bạn nhé!!!)
Áp dụng định luật bảo toàn khối lượng, ta có
mO2 = mP2O5 - mP= 142 - 62 = 80 gam
b/ => Khối lượng không khí đã đưa vào bình là:
mkhông khí = \(\frac{80.100}{25}\) = 320 gam
Chúc bạn học tốt!!!
a) Viết PTHH:
Bước 1: Viết sơ đồ phản ứng
P+ O2 ---> P2O5
Bước 2: Cân bằng số nguyên tử mỗi nguyên tố:
4 P+ 5 O2 ---> 2 P2O5
Bước 3: Viết PTHH
4 P+ 5 O2 -> 2 P2O5
Khối lượng của khi oxi khi tham gia phản ứng là:
Theo định luật bảo toàn khối lượng, ta có:
mP+ m(O2)= m(P2O5)
=> m(O2)= m(P2O5)- mP= 142-62=80 (g)
b) Khối lượng không khí đưa vào bình là:
mkhông khí= \(\frac{80.100}{25}\)= 320 (g)

a.
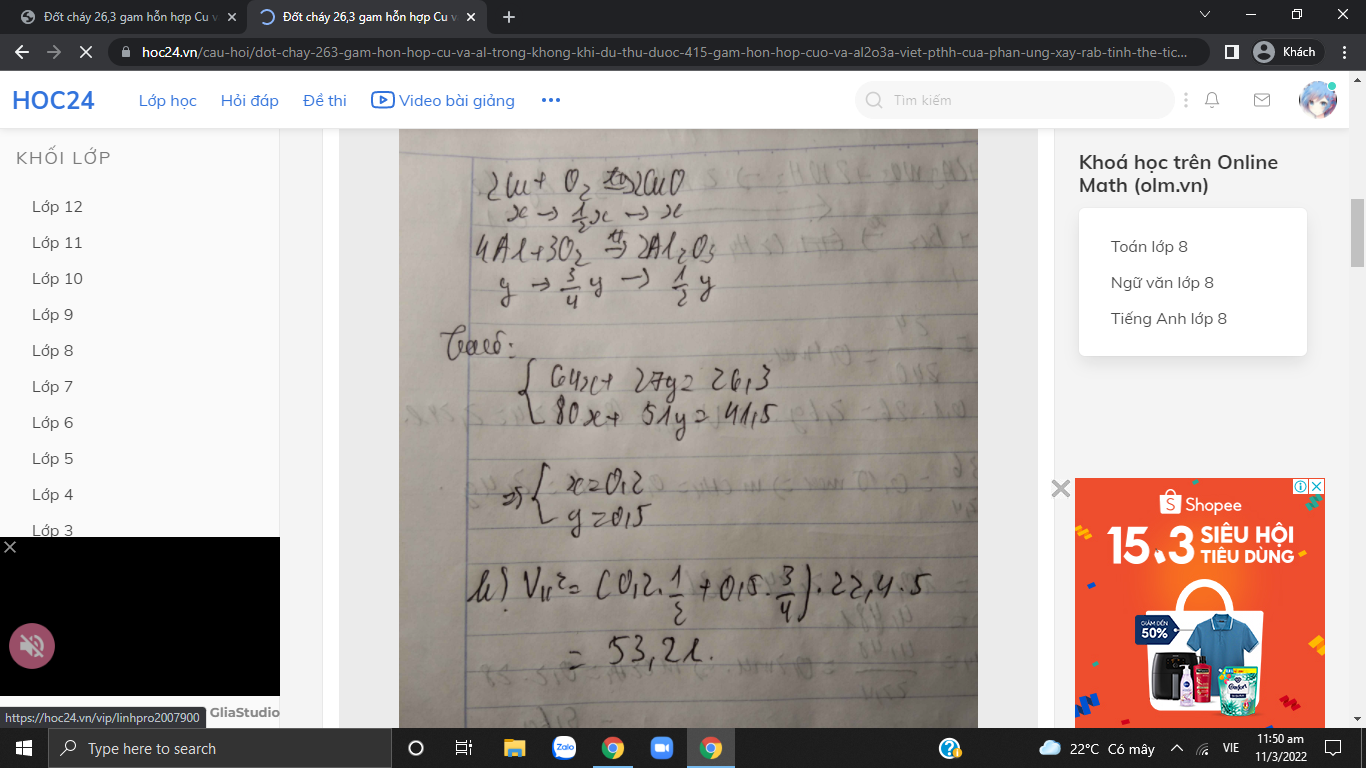
\(2Cu+O_2\rightarrow\left(t^o\right)2CuO\) \(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
x 1/2x x y 3/4y 1/2y ( mol )
Gọi \(\left\{{}\begin{matrix}n_{Cu}=x\\n_{Al}=y\end{matrix}\right.\)
Ta có:
\(\left\{{}\begin{matrix}64x+27y=26,3\\80x+\dfrac{1}{2}y.102=41,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,5\end{matrix}\right.\)
\(V_{kk}=\left(\dfrac{1}{2}.0,2+\dfrac{3}{4}.0,5\right).22,4.5=0,475.112=53,2l\)

a) PTHH: 2Cu + O2 ==(nhiệt)=> 2CuO
b) nCu = 6,4 / 64 = 0,1 (mol)
=> nO2 = 0,05 (mol)
=> VO2(đktc) = 0,05 x 22,4 = 1,12 lít
c) nCuO = nCu = 0,1 (mol)
=> mCuO = 0,1 x 80 = 8 (gam)
a) 2Cu + O2 ---> 2CuO
b) nCu = 6,4/64 =0,1 ( mol )
Theo PTHH : nO2 = 1/2 nCu = 0,1/2=0,05( mol )
VO2 = 0,05 x 22.4 = 1,12 ( l )
c)Theo PTHH : nCuO = nCu = 0,1 ( mol)
Khối lượng đồng oxit thu được sau phản ứng là : mCuO = 0,1 x 80 = 8 (g)

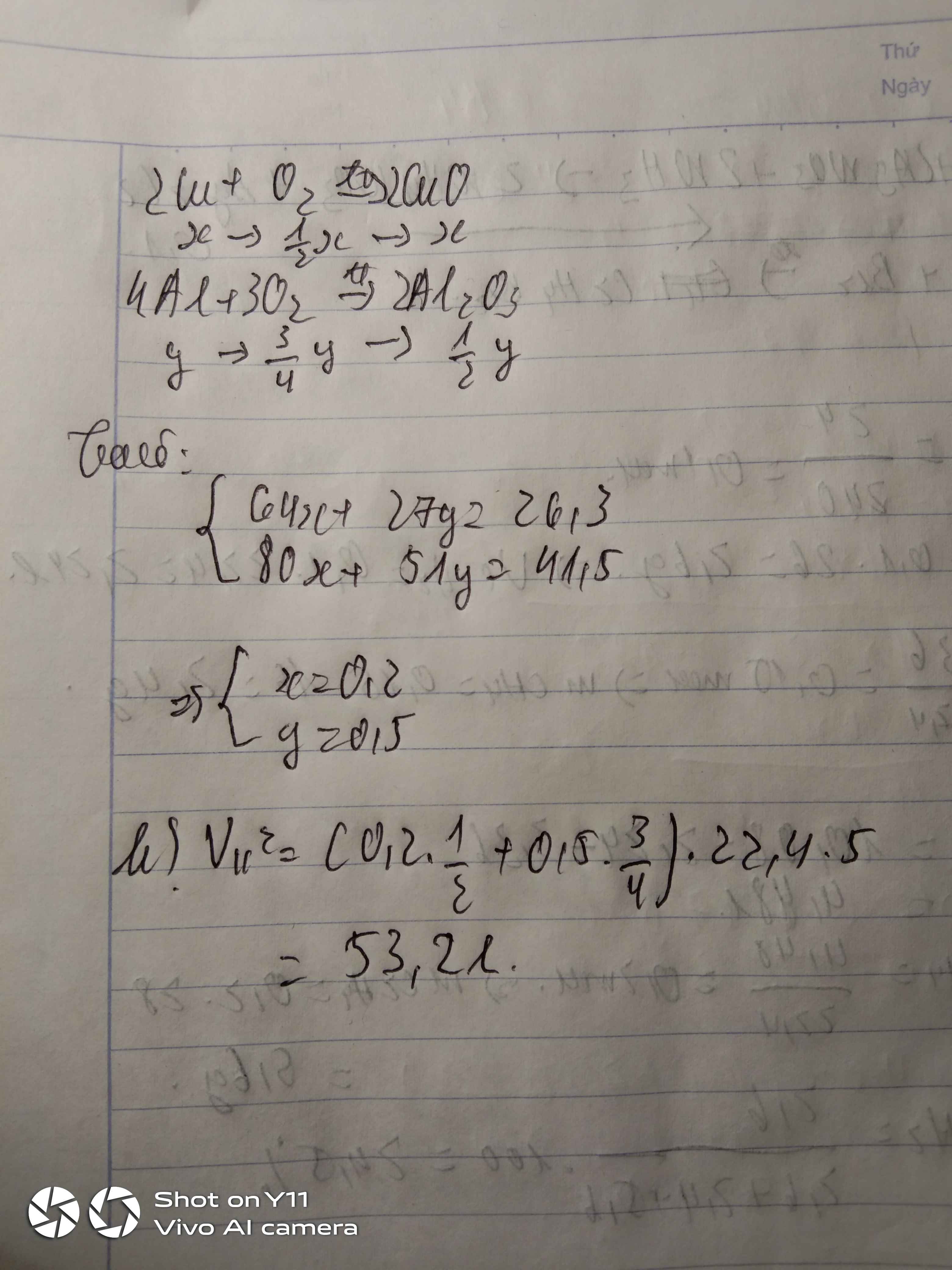

\(a)2Cu+O_2\xrightarrow[]{t^0}2CuO\)
\(b)n_{CuO}=a;n_{Cu\left(dư\right)}=b\\ 80.20\%a-64b=0\left(1\right)\\ n_{Cu\left(PƯ\right)}=n_{CuO}=a\\ 64a+64b=33,6\left(2\right)\\ \left(1\right)\&\left(2\right)\Rightarrow a=0,42;b=0,105\\ m_{Cu\left(pư\right)}=0,42.64=26,88g\\ n_{O_2}=\dfrac{1}{2}\cdot0,42=0,21mol\\ m_{O_2}=0,21.32=6,72g\\ c)m_{kk}=6,72:20\%=33,6g\)